Quand le verger rencontre la médecine régénératrice

Imaginez un instant que nous puissions réparer le corps humain, et plus spécifiquement le cartilage perdu, en utilisant une ressource aussi banale et abondante qu’une simple pomme. Ça paraît dingue, n’est-ce pas ? Pourtant, c’est exactement la piste incroyablement prometteuse qu’explore l’ingénierie tissulaire aujourd’hui. Face à des maladies qui nous font perdre des tissus essentiels, comme c’est le cas avec l’arthrose pour le cartilage ou l’ostéoporose pour l’os, le besoin de greffons est crucial, on ne le répétera jamais assez.
C’est dans ce contexte passionnant que le laboratoire Bioconnect de l’Université de Caen Normandie a fait une annonce fracassante. Moi-même, Karim Boumédiene, professeur de biochimie et biologie moléculaire et spécialiste en ingénierie tissulaire, j’ai le plaisir de diriger ce laboratoire avec le Pr Catherine Baugé. Nous avons récemment publié une étude détaillée dans la revue de référence, le Journal of Biological Engineering. Notre travail ? Nous avons réussi à combiner des cellules souches humaines avec des pommes qui avaient été préalablement « décellularisées » pour reconstruire du cartilage, tenez-vous bien, en laboratoire, c’est-à-dire in vitro ! C’est une approche vraiment fascinante.
L’ingénierie tissulaire : le défi de la reconstruction et l’énigme du rejet
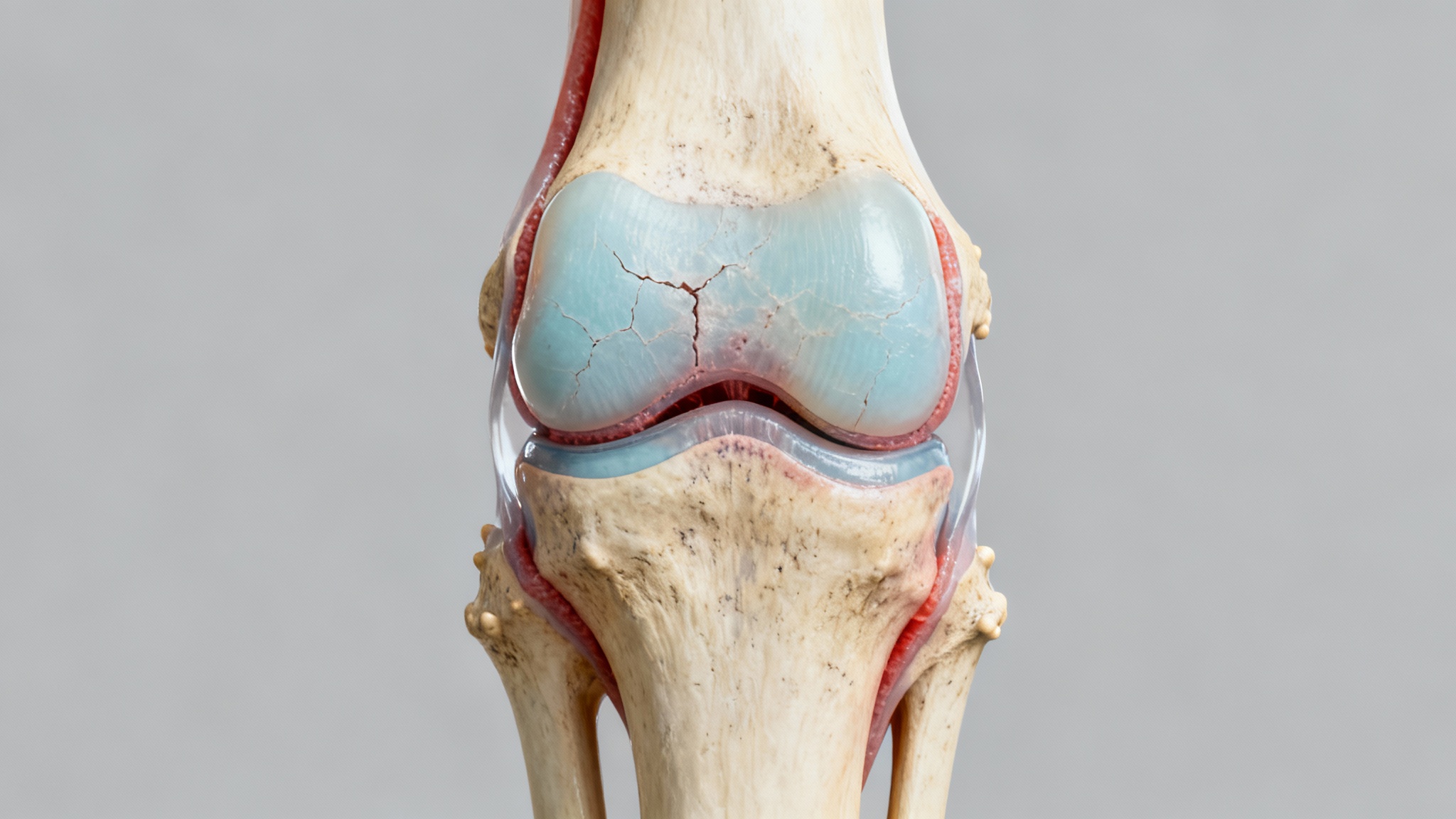
L’ingénierie tissulaire, c’est cette discipline incroyable qui a pour mission de reconstruire des tissus humains en laboratoire pour qu’ils servent de greffons, histoire de combler les pertes causées par des traumatismes ou des maladies dégénératives. En gros, la méthode est simple sur le papier : on prend des cellules du patient, on les implante dans un « biomatériau » et on fait incuber le tout dans des conditions parfaites pour former ce qu’on veut : os, muscle, ou notre fameux cartilage. C’est la solution rêvée, parce que les chirurgiens font face à un challenge colossal : la rareté des donneurs et surtout les problèmes de compatibilité.
D’ailleurs, c’est pour ça que la stratégie la plus efficace de l’ingénierie tissulaire consiste à utiliser, quand c’est possible, les propres cellules du patient. En les « ensemencant » sur le biomatériau, on contourne superbement les risques de rejet immunologique, qui sont un vrai cauchemar après une greffe traditionnelle. Il faut dire que trouver un tissu sain implantable, c’est souvent mission impossible.
La pomme, cet « échafaudage » végétal inattendu et ses avantages mondiaux

Alors, si cultiver des cellules en laboratoire est relativement facile, la vraie difficulté, c’est qu’elles ne s’organisent pas seules pour former un tissu avec du volume. Elles ont besoin d’un support, ce que l’on appelle un « échafaudage ». Avant, on utilisait des tissus humains ou des organes qui étaient « décellularisés » – on enlève les cellules pour ne garder que la matrice structurale – puis ensemencés avec des cellules saines. Mais attendez, cette stratégie a une limite évidente : il faut avoir accès à suffisamment de tissu humain de départ. Pas pratique, vous en conviendrez.
Heureusement, depuis une dizaine d’années, l’idée d’utiliser des tissus végétaux décellularisés a émergé comme une alternative géniale. L’étincelle, pour nous, ça a été la parution d’un article d’une équipe canadienne qui a montré, il y a quelques années, que la pomme décellularisée pouvait très bien s’entendre avec des cellules de mammifères. En tant que spécialistes du cartilage, on a tout de suite sauté sur l’occasion !
- Nous avons ainsi réalisé une première mondiale de reconstruction de cartilage avec un support d’origine végétale.
- Les avantages sont colossaux : la pomme, c’est une disponibilité quasi illimitée.
- Le prix est très faible.
- La biocompatibilité est déjà prouvée in vivo.
- Et surtout, on peut sculpter ce matériau comme on veut pour lui donner la forme exacte du tissu que l’on souhaite reconstruire.
De multiples applications : de la chirurgie à la fin de l’expérimentation animale

Évidemment, ce n’est qu’un premier pas ; il faut désormais passer par des étapes de validation rigoureuses. Nous devons d’abord réaliser des expériences précliniques sur l’animal, puis, si tout se passe bien, des essais cliniques sur l’humain pour s’assurer que ces tissus tiennent la route sur le long terme et apporteront un vrai bénéfice aux patients. Mais imaginez les possibilités ! Les applications potentielles sont nombreuses : nous pourrions réparer le cartilage articulaire après un microtraumatisme ou une arthrose. Mais aussi reconstruire le cartilage nasal (suite à un cancer ou un choc) ou même le cartilage auriculaire.
Mais attendez, il y a plus ! Notre étude ouvre aussi la voie à une réduction significative, voire un remplacement, des tests in vivo. Les tissus que nous construisons en laboratoire peuvent être utilisés pour modéliser les maladies de façon bien plus efficace grâce aux modèles dits « organoïdes ». On pourrait alors tester des traitements directement sur ces modèles, limitant ainsi le recours à l’expérimentation animale. C’est un gain éthique et scientifique indéniable.
Enfin, nous ne faisons que commencer à explorer l’immense potentiel du règne végétal. La pomme, c’était le point de départ, mais il y a une telle diversité ! Nous cherchons déjà d’autres végétaux, comme le céleri par exemple, pour déterminer quelle plante conviendrait le mieux à la reconstruction de tel ou tel tissu. L’avenir de la médecine régénératrice pourrait bien se trouver dans notre potager. Qui l’aurait cru ?
Ce contenu a été créé avec l’aide de l’IA.