Une avancée majeure venue d’Helsinki : un nouveau composé capable de « nettoyer » l’air de son dioxyde de carbone
Auteur: Mathieu Gagnon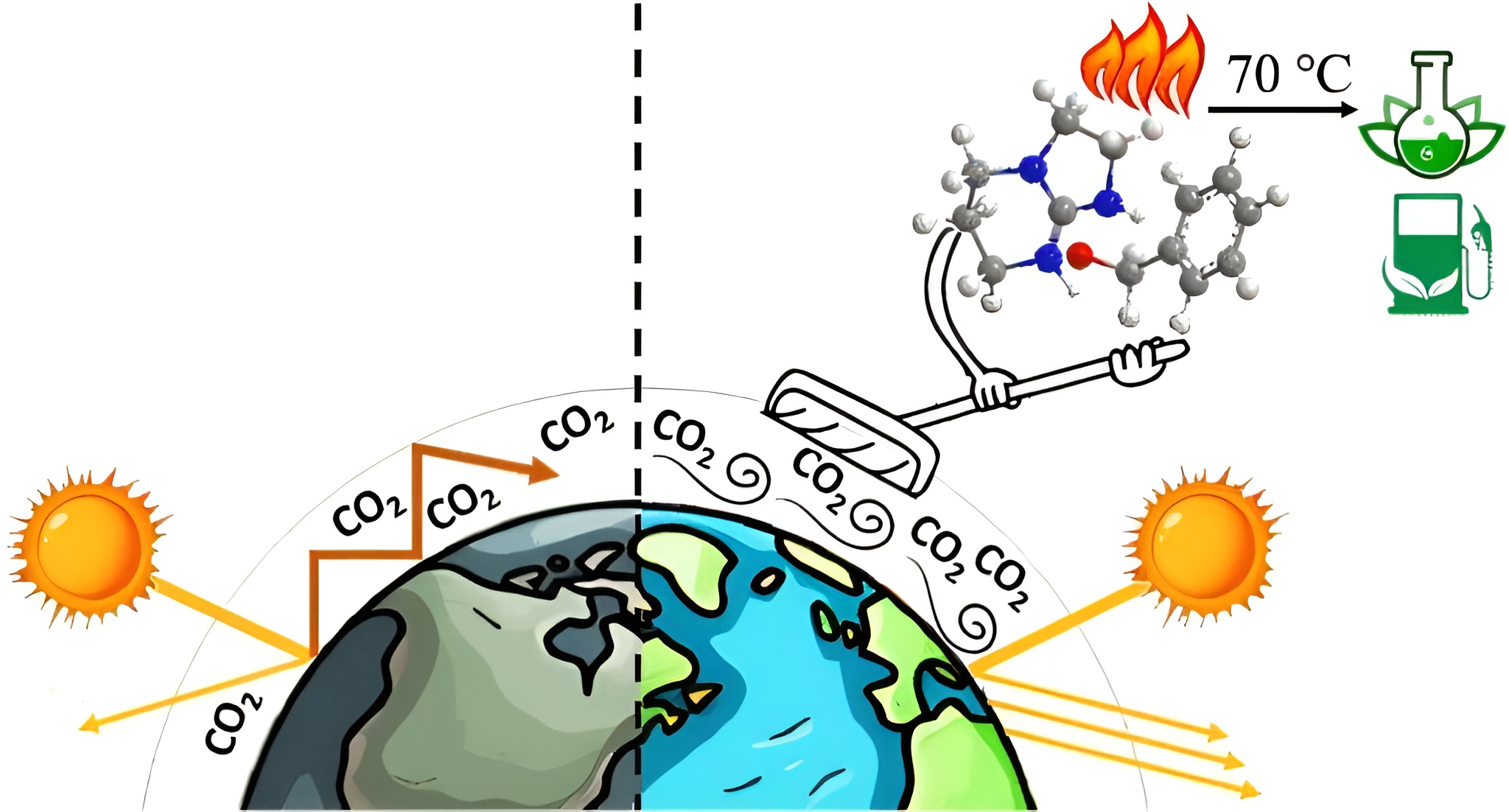
Une découverte prometteuse pour notre atmosphère

C’est fascinant de voir à quelle vitesse la recherche avance quand il s’agit de trouver des solutions pour notre planète. Une nouvelle méthode pour capturer le dioxyde de carbone directement dans l’air vient d’être mise au point, et c’est au département de chimie de l’Université d’Helsinki que cela se passe. On entend souvent parler de technologies complexes et lointaines, mais celle-ci semble avoir un ancrage très concret.
Les résultats de ces travaux ont d’ailleurs été publiés très récemment, en 2025 pour être précis, dans la revue spécialisée Environmental Science & Technology (vous pouvez retrouver l’étude sous le DOI 10.1021/acs.est.5c13908, si vous êtes du genre à aimer les détails techniques). Ce qui est intéressant ici, c’est l’approche utilisée par les chercheurs pour s’attaquer à ce fameux CO2 qui nous préoccupe tant.
Une efficacité redoutable et une chimie intelligente

Entrons un peu dans le vif du sujet, si vous le voulez bien. La méthode a été développée par une chercheuse postdoctorale, Zahra Eshaghi Gorji, qui a basé son travail sur un mélange assez spécifique : un composé fait d’une superbase et d’alcool. Les tests, qui ont été menés au sein du groupe du professeur Timo Repo, montrent des résultats qui, ma foi, semblent vraiment prometteurs. Tenez-vous bien : un seul petit gramme de ce composé est capable d’absorber 156 milligrammes de dioxyde de carbone. Et le plus beau ? Il le fait directement à partir de l’air ambiant non traité. C’est une performance qui surpasse clairement les méthodes de capture du CO2 que nous utilisons actuellement.
Mais ce n’est pas tout. Ce qui m’a particulièrement marqué en lisant ces résultats, c’est la sélectivité du produit. C’est un peu comme s’il avait des œillères : le composé ne réagit absolument pas avec l’azote, l’oxygène ou les autres gaz atmosphériques. Il ne vise que le CO2. C’est une distinction cruciale pour l’efficacité du processus.
Là où cette innovation devient vraiment révolutionnaire, c’est au moment de relâcher ce gaz capturé. Habituellement, avec les composés actuels, il faut chauffer à des températures infernales, souvent au-delà de 900° C. Ici ? Il suffit de chauffer le composé à 70° C pendant 30 minutes. C’est tout. Le CO2 propre est alors récupéré et peut être recyclé. C’est, à mon avis, l’avantage clé de cette découverte : une facilité de relâchement déconcertante qui économise énormément d’énergie.
Durabilité, composition et passage à l’échelle industrielle

Bien sûr, on peut se demander si ce produit tient la route sur la durée. Selon Zahra Eshaghi Gorji, le composé peut être utilisé plusieurs fois, même si l’usure finit par se faire sentir. Il conserve 75 % de sa capacité d’origine après 50 cycles, et cela descend à 50 % après 100 cycles. Ce n’est peut-être pas éternel, mais c’est déjà une belle performance pour un début. D’ailleurs, ce résultat ne s’est pas fait en un jour : il a fallu expérimenter avec de nombreuses bases pendant plus d’un an au total pour en arriver là.
Alors, de quoi est faite cette « potion » magique ? La base la plus prometteuse s’est révélée être le 1,5,7-triazabicyclo [4.3.0] non-6-ene (qu’on appelle TBN pour faire plus simple, heureusement !). Ce TBN a été développé dans le groupe du professeur Ilkka Kilpeläinen et a été combiné avec de l’alcool benzylique pour produire le composé final. La bonne nouvelle, c’est que Zahra Eshaghi Gorji note qu’aucun de ces composants n’est coûteux à produire. De plus, le fluide est non toxique, ce qui est toujours rassurant.
Et maintenant ? Les chercheurs ne comptent pas s’arrêter aux tests en laboratoire. Le composé va être testé dans des usines pilotes, à une échelle quasi industrielle. Fini les grammes, on passe aux choses sérieuses. Pour cela, il faudra toutefois transformer ce liquide en version solide. L’idée, comme l’explique Gorji, est de lier le composé à des substances comme la silice et l’oxyde de graphène, ce qui favorise l’interaction avec le dioxyde de carbone.
Conclusion : Un pas de plus vers un air plus pur

En somme, cette découverte de l’Université d’Helsinki nous montre qu’il existe des solutions alternatives, moins énergivores et plus sûres, pour traiter le problème du carbone atmosphérique. Bien sûr, il reste l’étape cruciale de l’industrialisation, mais savoir que l’on peut capturer du CO2 à 70° C au lieu de 900° C laisse entrevoir des perspectives réjouissantes pour l’avenir de ces technologies.
Ce contenu a été créé avec l’aide de l’IA.