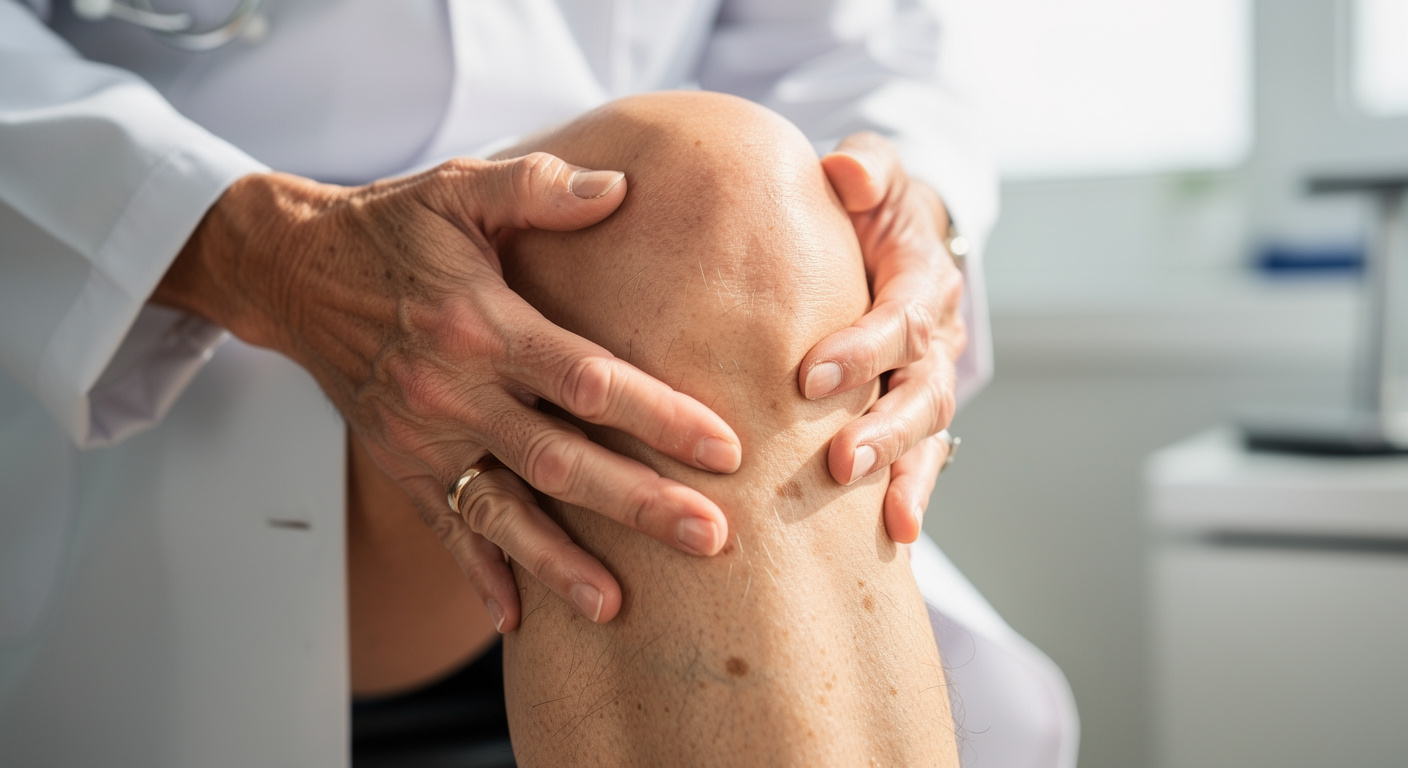
Stimuler les bonnes bactéries intestinales via des interventions ciblées pourrait ralentir le déclin cognitif
Auteur: Mathieu Gagnon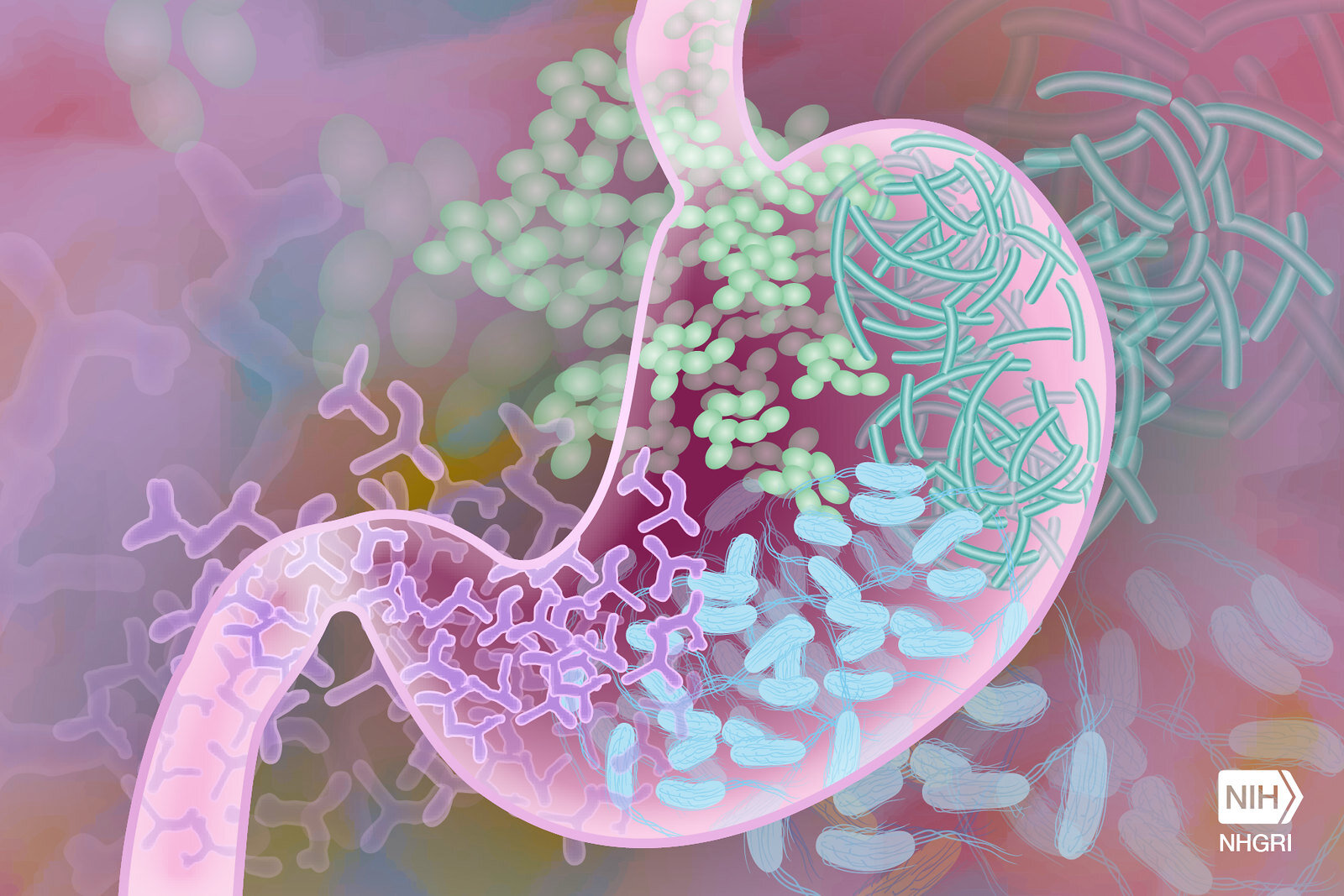
L’axe intestin-cerveau : une autoroute de l’information
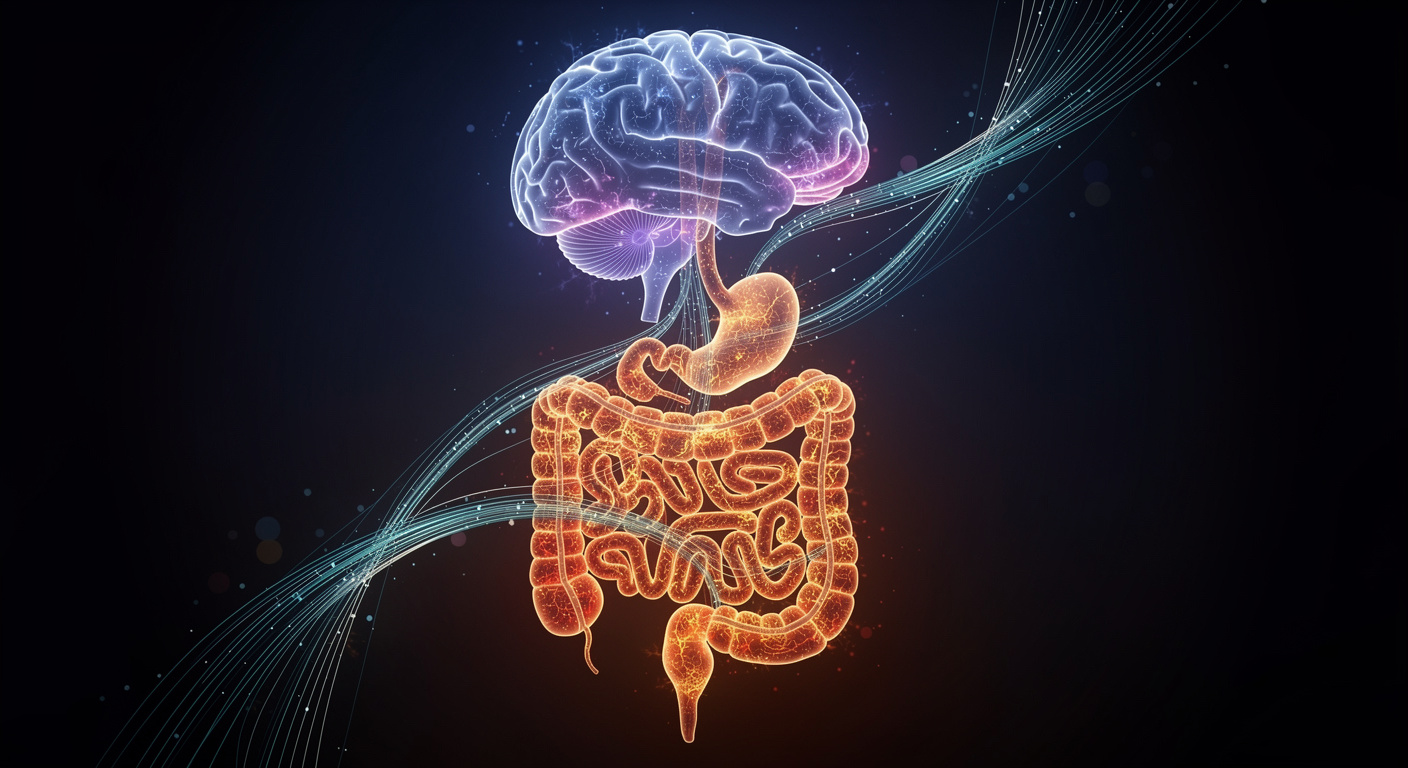
L’origine des maladies neurodégénératives, telles que la maladie d’Alzheimer ou la démence, ne se limite pas aux seules frontières du cerveau. L’état de notre système digestif a la capacité de déclencher silencieusement un cycle d’inflammation chronique à l’échelle de tout l’organisme. Ce processus inflammatoire va ensuite pousser le cerveau vers le déclin cognitif, soulevant une question fondamentale : comment la pathogenèse d’une maladie en apparence purement cérébrale peut-elle débuter dans un organe principalement occupé à produire des substances chimiques pour digérer la nourriture ?
La réponse réside dans l’axe intestin-cerveau. Ces deux entités sont reliées par une véritable autoroute de la communication à double sens, qui envoie en permanence des signaux entre le tube digestif et le système nerveux central. Cette connexion physique et chimique fonctionne sans interruption pour maintenir l’équilibre de l’organisme.
Ce réseau de communication repose sur des messagers chimiques spécifiques, tels que les neurotransmetteurs et les acides gras. En échangeant continuellement ces informations, l’axe intestin-cerveau façonne directement notre mémoire, régule notre humeur et contrôle nos déclencheurs d’inflammation.
Un écosystème microscopique aux conséquences immenses
L’intestin fonctionne comme un écosystème anaérobie complexe, grouillant d’un vaste mélange de micro-organismes. On y trouve des bactéries, des champignons et des protozoaires, un ensemble collectivement appelé le microbiote. Ces organismes s’installent dans différentes régions de la paroi intestinale pour former la majeure partie du microbiome humain, lequel englobe plus de 1 000 espèces microbiennes distinctes.
De nombreuses études ont déjà établi que ce microbiote intestinal joue un rôle clé dans le développement du cerveau et la cognition. Au fil du temps, à mesure que les personnes vieillissent ou adoptent une mauvaise alimentation, cette communauté de bactéries peut se transformer. Les souches utiles cèdent la place à des souches nocives, créant un état de déséquilibre médicalement appelé dysbiose.
Ces déséquilibres dans la flore intestinale alimentent discrètement le déclin cérébral. La dysbiose déclenche des inflammations, affaiblit la barrière protectrice du cerveau et permet à des protéines nocives, étroitement liées à la maladie d’Alzheimer, de s’accumuler de manière dangereuse.
Une analyse internationale d’une ampleur inédite

Jusqu’à présent, la plupart des recherches se concentraient sur les traitements du microbiote intestinal de manière isolée, en étudiant une seule approche à la fois. Une récente étude, dont les résultats sont publiés dans la revue Nutrition Research, a choisi d’adopter une vue d’ensemble. Les chercheurs ont voulu comprendre comment les régimes spécialisés, les probiotiques et les greffes améliorent le microbiote intestinal, tout en comparant leur efficacité respective.
Pour mener à bien ce travail de fond, l’équipe a examiné les données de personnes âgées de plus de 45 ans souffrant de problèmes de mémoire. Ils ont pris en compte les traitements qui ciblent directement ou indirectement les bactéries intestinales, tout en mesurant les résultats cognitifs à l’aide de tests validés de la fonction cérébrale.
Après avoir passé au crible des milliers d’études réparties dans cinq grandes bases de données médicales, les scientifiques ont réduit leur liste aux 15 essais cliniques les plus pertinents. Ces travaux proviennent d’Europe, d’Asie, d’Amérique du Nord et du Moyen-Orient, et ont impliqué un total précis de 4 275 participants.
De l’assiette à la greffe : les interventions testées
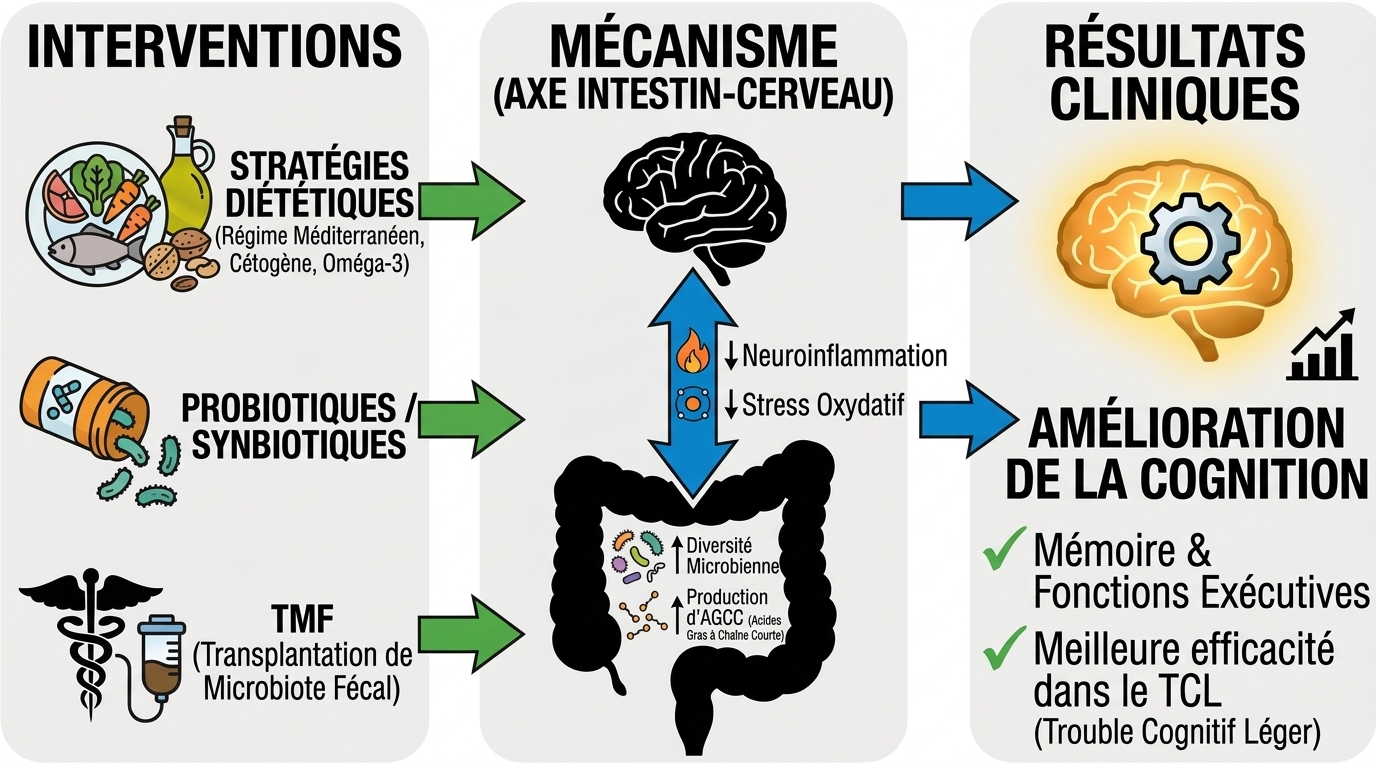
L’analyse menée sur ces 4 275 individus a exploré les effets de plusieurs approches différentes. Parmi les stratégies nutritionnelles, les chercheurs se sont penchés sur le régime méditerranéen, riche en plantes et en graisses saines, ainsi que sur le régime cétogène, caractérisé par une faible teneur en glucides et une forte teneur en graisses. Les données montrent que ces régimes ont amélioré les performances cognitives en remodelant le microbiote intestinal et en augmentant la présence de produits chimiques neuroprotecteurs comme le GABA.
L’étude s’est également intéressée à la supplémentation, incluant l’apport de probiotiques, d’oméga-3 et de symbiotiques. Du côté des interventions médicales, les essais ont évalué la transplantation de microbiote fécal, ou TMF, une procédure consistant à transférer des bactéries intestinales saines provenant d’un donneur vers un patient.
Les résultats démontrent que la stimulation de l’intestin par les probiotiques, et tout particulièrement par la transplantation de microbiote fécal, s’est traduite par une meilleure fonction cognitive. La TMF s’est distinguée en entraînant les changements les plus rapides et les plus spectaculaires sur la santé intestinale. De manière générale, le fait de moduler le microbiote via ces différentes voies contribue à améliorer la mémoire, la fonction exécutive et la performance cognitive globale, s’imposant comme une voie non médicamenteuse pour soutenir la santé du cerveau.
Changements biologiques et importance cruciale du dépistage précoce

Le succès de cet effet protecteur est attribuable à une augmentation des bactéries intestinales bénéfiques. Ces dernières produisent des composés capables de ralentir le déclin cognitif. L’ensemble des interventions testées a déclenché des changements biologiques positifs chez les participants, notamment une plus grande diversité microbienne, une production accrue d’acides gras à chaîne courte et une diminution de l’inflammation cérébrale, autant d’acteurs travaillant de concert pour un cerveau en meilleure santé.
Toutefois, l’équipe de recherche a observé des limites dans l’application de ces traitements. Les régimes alimentaires et les interventions axées sur l’intestin ont montré des avantages clairs dans les cas de déficience cognitive précoce ou légère. À l’inverse, leur impact s’est révélé limité chez les patients atteints d’une forme avancée de la maladie d’Alzheimer.
Cette observation met en lumière la fenêtre d’action optimale pour ces traitements. Comme l’indiquent les chercheurs en conclusion de leur analyse : bien que les résultats soutiennent les interventions sur l’intestin comme un outil puissant pour ralentir le déclin cognitif, le moment choisi est primordial — plus on commence tôt, mieux cela fonctionne.
Selon la source : medicalxpress.com