Cancer de l’œil : une approche surprenante utilisant le sperme de porc pour améliorer l’efficacité des traitements
Auteur: Adam David
L’obstacle des barrières oculaires face au cancer infantile

Le rétinoblastome représente la forme la plus fréquente de cancer oculaire chez l’enfant, bien qu’il demeure une tumeur maligne rare. La prise en charge de cette pathologie se heurte à un obstacle anatomique majeur. Si les substances thérapeutiques actuelles possèdent la capacité d’éliminer la maladie, leur administration se trouve complexifiée par la grande fragilité des tissus qui composent l’œil.
La structure oculaire possède un système de défense particulièrement robuste. Le segment postérieur de l’œil bénéficie d’une protection naturelle assurée par un ensemble complexe de barrières biologiques. La barrière hémato-rétinienne, par exemple, bloque efficacement la pénétration des particules étrangères. Pour atteindre la tumeur située en profondeur, les traitements doivent impérativement franchir au moins l’une de ces lignes de défense.
Les protocoles médicaux classiques reposent sur des approches souvent éprouvantes pour les jeunes patients. Les médecins ont recours aux injections intravitréennes, à la radiothérapie, à la cryothérapie ou à la chimiothérapie systémique. Ces actes médicaux s’avèrent douloureux et s’accompagnent de graves effets secondaires. Dans certaines situations, ces traitements peuvent entraîner une perte de vision permanente.
Les limites des méthodes traditionnelles et l’alternative des vésicules
Pour contourner les limites anatomiques de l’œil, la communauté scientifique étudie de nouveaux vecteurs de transmission. Une recherche récente publiée dans la revue Science Advances met en évidence une approche singulière : l’exploitation d’exosomes extraits de sperme de porc. Cette méthode inédite s’annonce potentiellement plus sûre et moins invasive que les interventions chirurgicales ou chimiques actuelles.
L’utilisation de véhicules médicamenteux n’est pas nouvelle, les scientifiques ayant déjà testé des microsphères lipidiques pour acheminer le traitement du rétinoblastome. Ces tentatives passées affichent un bilan mitigé. Leur efficacité reste limitée par une faible capacité à transporter le principe actif, une sélectivité insuffisante pour cibler la maladie, ainsi qu’une toxicité non négligeable pour l’organisme. À l’inverse, les exosomes apportent des caractéristiques techniques particulièrement adaptées.
Ces vésicules extracellulaires nanométriques sont produites naturellement par les cellules pour véhiculer des molécules. Elles se distinguent par leur biocompatibilité, une faible immunogénicité et une grande aptitude à traverser les barrières biologiques. Les exosomes issus du sperme possèdent une capacité naturelle à infiltrer des structures complexes grâce à un profil de protéines spécifiques. Les auteurs de l’étude valident cette observation : « Ces protéines permettent aux exosomes dérivés du sperme de franchir des barrières biologiques considérables, ce qui suggère qu’ils pourraient posséder des propriétés intrinsèques favorisant la pénétration des barrières oculaires. Cette capacité unique fait des exosomes dérivés du sperme un vecteur intéressant pour l’administration non invasive de médicaments au segment postérieur de l’œil ». Jusqu’alors, la littérature scientifique se concentrait essentiellement sur l’injection de ces vésicules, laissant le domaine des soins non invasifs inexploré.
La composition novatrice d’un collyre expérimental

L’équipe de recherche a concrétisé cette hypothèse par le développement de gouttes ophtalmiques. La préparation liquide repose sur l’association des exosomes dérivés de sperme porcin avec de l’acide folique, couramment appelé AF. Cette base intègre un composé nanoenzymatique identifié sous l’acronyme CMG.
L’architecture de ce système CMG regroupe trois éléments distincts : des points quantiques de carbone, du dioxyde de manganèse et de la glucose oxydase. Les exosomes agissent comme une enveloppe qui encapsule l’ensemble de ces composants. Leur rôle mécanique s’avère déterminant. Ils provoquent l’ouverture de brèches au niveau des jonctions serrées qui consolident les structures protectrices de l’œil, de manière totalement temporaire et réversible, facilitant le passage du principe actif.
L’acide folique intervient pour diriger le traitement avec précision. Sa présence optimise le repérage des cellules tumorales. L’observation de l’application de ce collyre montre que les vésicules trouvent leur chemin à travers les tissus oculaires en empruntant deux trajectoires biologiques majeures : la voie cornéenne d’une part, et la voie conjonctivale d’autre part.
Le mécanisme d’action ciblé contre les cellules tumorales
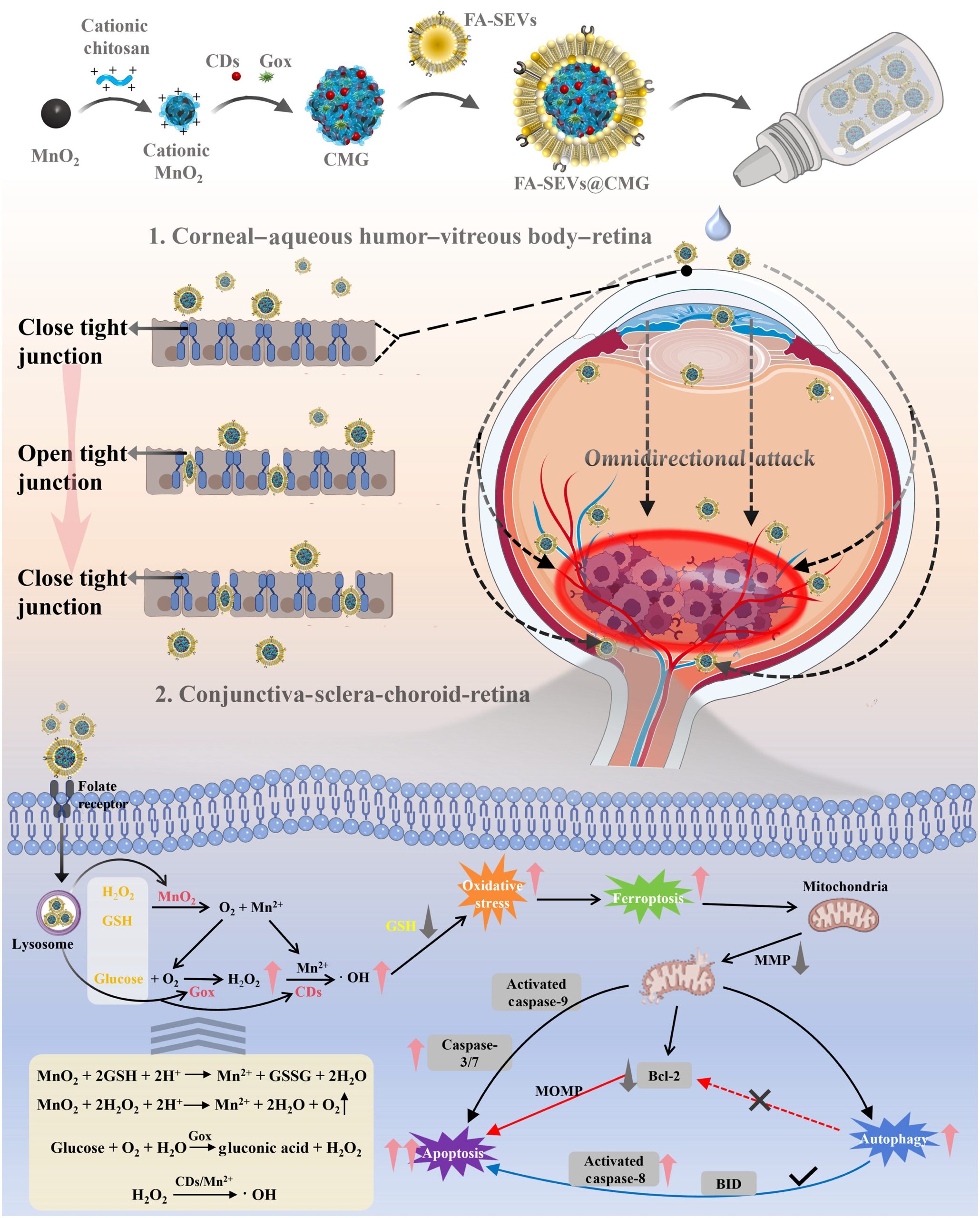
Une fois les défenses anatomiques franchies, le traitement initie son attaque contre la maladie. Selon les données partagées par les scientifiques, le complexe CMG génère un stress oxydatif élevé à l’intérieur même des cellules tumorales. Ce processus induit la destruction autonome de la tumeur.
L’un des avantages observés réside dans la préservation de l’environnement immédiat de la zone traitée. La réaction chimique provoquée par le collyre épargne les tissus sains documentés dans le modèle d’étude. La combinaison entre le vecteur animal et le traceur de ciblage crée une synergie essentielle à cette précision. Les chercheurs confirment cette dynamique : « Ce collyre exploite la capacité de pénétration des exosomes dérivés du sperme et l’effet de ciblage de l’acide folique pour améliorer l’administration de médicaments aux cellules du rétinoblastome ».
L’action combinée du stress oxydatif provoqué par le CMG et des brèches temporaires créées par les exosomes dessine une nouvelle modalité d’action thérapeutique. L’approche offre la possibilité d’atteindre le cœur du problème oncologique sans compromettre l’intégrité globale de l’organe de la vue.
Une efficacité mesurée avec précision sur des modèles in vivo
L’efficacité du dispositif a été mesurée in vivo grâce à des modèles de souris porteuses de tumeurs oculaires. Les chercheurs ont divisé les animaux en plusieurs catégories pour isoler les effets de chaque composé. Le premier groupe a bénéficié du traitement complet, le deuxième a reçu le système CMG sans le vecteur exosomique, et le dernier groupe n’a été soumis à aucune intervention médicale.
Au bout de 30 jours de suivi, les rongeurs ayant reçu le collyre intégral ont affiché une réduction drastique de la taille de leur tumeur, affichant des résultats nettement supérieurs à ceux traités par le CMG isolé. L’observation des sujets soignés avec la formule complète révèle la présence d’environ 2,35 % de masse tumorale résiduelle en comparaison avec les souris non traitées.
L’analyse structurelle des yeux des souris a soulevé d’autres bénéfices. Les animaux laissés sans traitement présentaient une forte néovascularisation et une opacité intraoculaire aggravée. Les individus soignés avec la combinaison médicamenteuse complète comprenant les exosomes et l’acide folique conservaient une transparence oculaire proche de la normale à l’issue de la période de 30 jours.
Les étapes futures et les défis de l’application clinique
Les résultats obtenus avec ce collyre ouvrent des perspectives pour traiter diverses pathologies du système visuel. L’équipe de recherche avance que le modèle d’administration utilisant des exosomes porcins pourrait s’étendre à d’autres affections altérant la vue. La dégénérescence maculaire liée à l’âge (DMLA) et la rétinopathie diabétique figurent parmi les cibles médicales envisagées pour de futures expérimentations.
L’arrivée de ce traitement dans les hôpitaux n’est pas immédiate. Le passage à des essais cliniques sur l’homme nécessite des investigations approfondies pour valider la fiabilité absolue de ce vecteur biologique. L’industrialisation de ce procédé médical implique de résoudre des problématiques liées au matériel vivant.
La production à grande échelle d’exosomes issus du sperme représente un défi logistique et sanitaire. Les biologistes constatent d’importantes variations entre les différents lots produits en laboratoire. Ils soulèvent le maintien d’une certaine immunogénicité persistante et pointent des risques de contamination par des agents pathogènes inhérents à la manipulation de ces extraits animaux.
Selon les sources : trustmyscience.com | Science Advances