Certains amphibiens peuvent régénérer des membres perdus : une simple méthode pourrait être un premier pas pour activer ce pouvoir chez les mammifères
Auteur: Mathieu Gagnon
Le mystère persistant de la cicatrisation animale

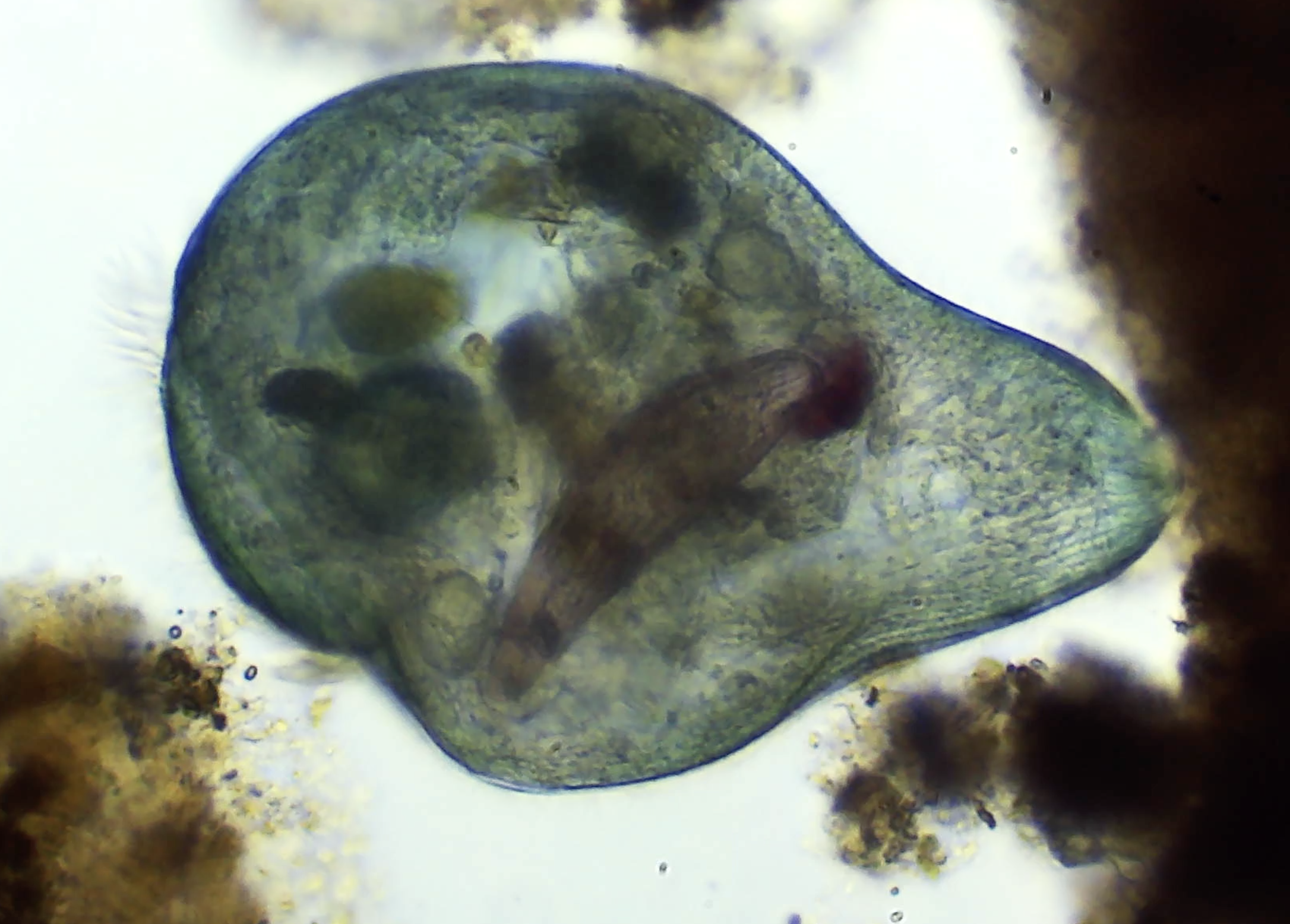
C’est un mystère persistant qui fascine la communauté scientifique. Pourquoi certains amphibiens, tels que les salamandres et les têtards de grenouilles, parviennent-ils à régénérer un membre perdu alors que les mammifères en sont incapables ? Pendant des décennies, les chercheurs ont tenté de percer le secret de cette différence fondamentale, mais le problème posé par l’amputation les a systématiquement laissés sans réponse.
Aujourd’hui, des travaux menés par des scientifiques de l’École Polytechnique Fédérale de Lausanne (EPFL) offrent un regard inédit sur ce phénomène. Leurs recherches se concentrent sur un facteur totalement inattendu : l’oxygène. Bien que ces découvertes n’en soient qu’à leurs balbutiements, elles portent l’espoir d’ouvrir à terme de nouvelles voies pour améliorer la cicatrisation des plaies chez l’être humain.
La régénération des membres trouve son origine première dans le processus même de la cicatrisation. Dès qu’un membre est amputé, les cellules situées autour de la zone blessée commencent à colmater la plaie et adoptent des profils de cellules régénératives. Si l’enchaînement se déroule de manière fluide, dans le bon organisme, il aboutit à la repousse intégrale du membre manquant. C’est exactement le scénario qui se joue chez les amphibiens. Toutefois, si la machine s’enraye — le lot quotidien des humains et des autres mammifères —, la plaie se referme beaucoup plus lentement. Ce délai laisse le champ libre à la formation de cicatrices qui finissent par bloquer définitivement toute tentative de régénération.
La mécanique des cellules et le prix du sang chaud
Au fil des années, les biologistes ont avancé plusieurs explications concurrentes pour justifier l’arrêt prématuré de ce processus chez les mammifères. L’une des hypothèses majeures suggère une défaillance dans la fabrication des cellules régénératives. Lors d’une blessure, l’amphibien possède la capacité stupéfiante de « dédifférencier » ses cellules. Il transforme des cellules osseuses ou musculaires spécifiques pour les faire revenir à l’état de cellules souches. Ces dernières migrent ensuite vers la plaie pour constituer un blastème, un amas de cellules non différenciées servant de véritable progéniteur à la régénération.
Ce subtil remodelage cellulaire n’a tout simplement pas lieu chez l’homme. Face à une blessure, notre organisme dicte une urgence absolue : refermer la plaie à l’aide d’un tissu cicatriciel épais. Cette fibrose répond à un double impératif de survie immédiate visant à stopper les saignements et à prévenir l’invasion d’infections.
Une approche alternative s’appuie sur l’histoire évolutive de la thermorégulation pour comprendre pourquoi les amphibiens réussissent là où les mammifères échouent. Cet argument postule que l’acquisition d’une température corporelle chaude et constante par les mammifères a constitué une avancée majeure, mais qu’elle nous aurait incidemment coûté notre aptitude à faire repousser nos membres perdus.
L’oxygène, le déclencheur insoupçonné

Le rôle de l’environnement physique mérite une attention particulière. Un constat s’impose : de nombreuses espèces dotées de compétences régénératrices vivent dans des milieux aquatiques. Les larves d’amphibiens débutent leur existence immergées dans l’eau, un milieu naturel où les niveaux d’oxygène se révèlent nettement inférieurs à ceux présents dans l’air. À l’inverse, les tissus d’un mammifère blessé subissent immédiatement l’exposition aux niveaux d’oxygène particulièrement élevés du monde terrestre.
Si cette disparité environnementale est connue de longue date, une question demeurait sans réponse : cette situation n’était-elle qu’une simple conséquence du mode de vie, ou jouait-elle un rôle direct et actif dans la régénération des membres ? La nouvelle étude apporte un éclairage décisif en démontrant que l’oxygène exerce bel et bien une influence cruciale. En comparant des membres amputés de têtards de grenouilles et d’embryons de souris, l’équipe a mis en évidence que la façon dont les cellules détectent l’oxygène dicte directement le déclenchement de la régénération.
« Pendant longtemps, la recherche sur la régénération s’est concentrée sur les amphibiens, tandis que la régénération des mammifères était rarement examinée expérimentalement côte à côte de manière comparable », a expliqué Can Aztekin de l’EPFL dans un communiqué. Le scientifique précise : « Bien que de nombreuses études aient montré que les espèces capables de régénération comme les amphibiens et les mammifères partagent des gènes similaires, ce qui suggère que les mammifères pourraient conserver une capacité de régénération latente, il restait difficile de savoir si les tissus des mammifères peuvent effectivement activer des programmes de régénération des membres, et ce qui les empêche de le faire. »
Une plongée au cœur de la mécanique cellulaire
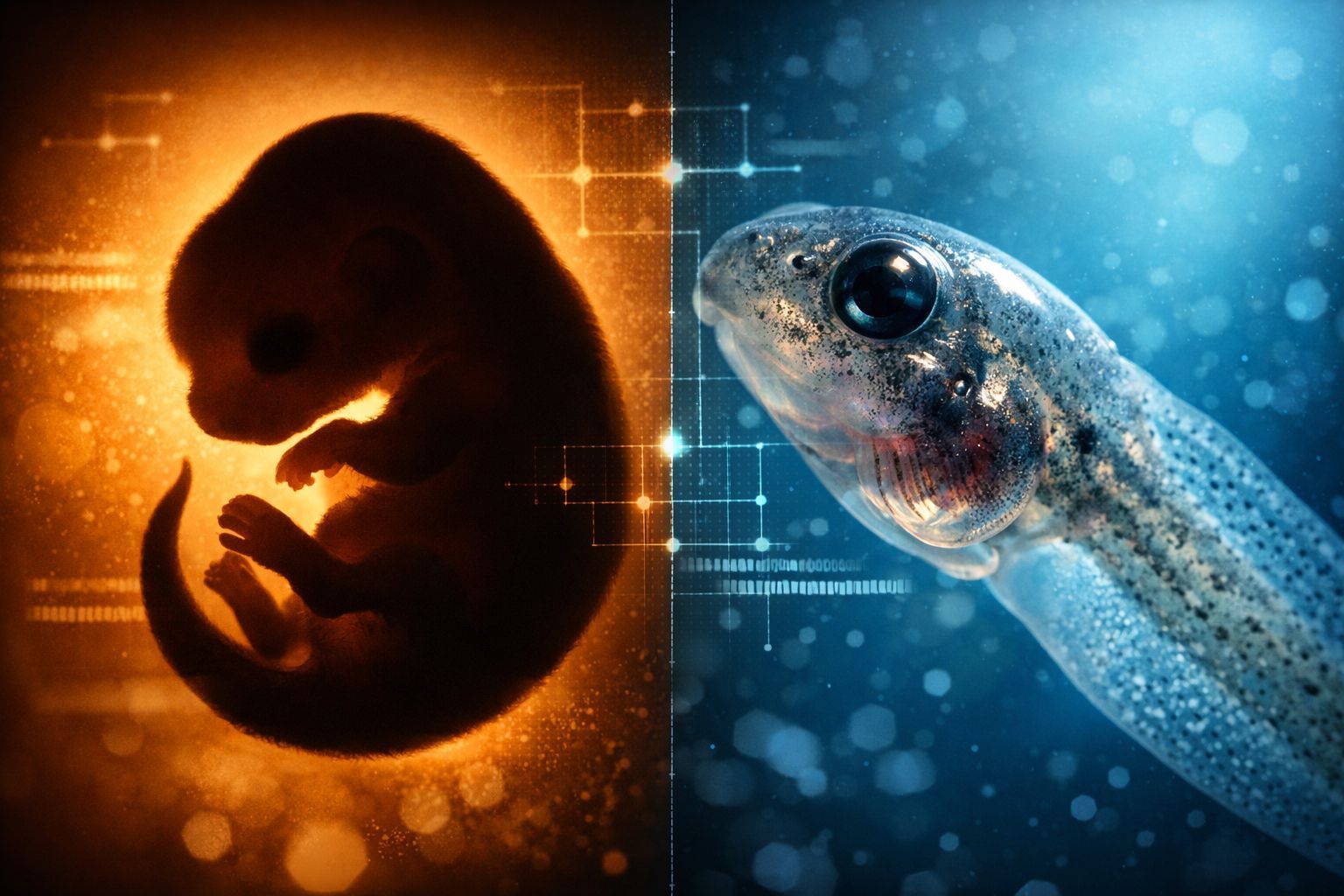
Pour mener à bien cette recherche, Can Aztekin et ses collègues ont procédé à l’amputation de membres en développement de têtards de grenouilles et d’embryons de souris. Ces minuscules membres ont ensuite été mis en culture à l’extérieur du corps, sous des conditions d’oxygénation rigoureusement contrôlées. Une partie des échantillons a été placée sous de faibles niveaux d’oxygène, imitant l’environnement aquatique, tandis que le reste a été soumis à des niveaux d’oxygène élevés, proches de ceux de l’air ambiant. L’équipe a scruté la réaction des cellules sous toutes ses coutures en mesurant la vitesse de fermeture de la plaie, le mouvement cellulaire, l’activité génétique, le métabolisme, ainsi que les états épigénétiques, c’est-à-dire les modifications affectant l’emballage de l’ADN.
L’analyse a mis en exergue le rôle fondamental d’une protéine nommée HIF1A, chargée de réguler les réponses des cellules face à une carence en oxygène. Lorsque l’oxygène baisse, cette protéine gagne en stabilité et active un ensemble de programmes initiant les processus de cicatrisation et de régénération autour d’une blessure. L’équipe a découvert que l’abaissement des niveaux d’oxygène engendrait un impact particulièrement net sur les membres des embryons de souris. Placées dans cette condition spécifique, leurs cellules refermaient les blessures avec plus de vélocité et semblaient s’engager sur la voie d’un programme régénératif. En stabilisant artificiellement la protéine HIF1A, les chercheurs ont reproduit ces mêmes effets positifs, y compris lorsque l’environnement demeurait saturé d’oxygène.
Le manque d’oxygène a provoqué des répercussions spectaculaires au niveau cellulaire. La vitesse de cicatrisation s’est accrue et le comportement des cellules cutanées s’est métamorphosé. Devenues plus mobiles, ces cellules de la peau ont démontré une capacité à modifier leurs propriétés mécaniques. Simultanément, le métabolisme global a basculé vers la glycolyse, un processus de nature anaérobie qui se manifeste lors des situations de privation d’oxygène. L’équipe a relevé une ultime transformation : les marques chimiques présentes sur les protéines associées à l’ADN ont été altérées pour privilégier l’activation des gènes directement liés à la régénération.
La promesse d’une médecine révolutionnée

Le comportement observé chez les têtards de grenouilles dresse un tableau radicalement différent. Leurs membres amputés se sont régénérés avec une remarquable efficacité face à un large spectre de niveaux d’oxygène, y compris dans des conditions surpassant largement celles rencontrées à l’air libre. Leurs cellules réussissent la prouesse de conserver une activité stable de la protéine HIF1A même en présence d’une forte concentration d’oxygène. Cette résilience s’explique par une très faible expression des gènes qui s’occupent habituellement de désactiver cette voie biochimique.
Tout au long de ces recherches parues dans la revue Science, les biologistes ont acquis une certitude : les amphibiens capables de régénération font preuve d’une capacité très réduite à détecter l’oxygène, un atout qui permet à leur programme de régénération de s’amorcer et de se maintenir dans le temps. À l’exact opposé, les cellules des mammifères testés, humains comme souris, ont réagi vigoureusement à la présence d’oxygène, provoquant la désactivation précipitée de leurs programmes régénératifs après l’amputation. Ce constat indique que les membres des mammifères hébergent bel et bien un potentiel de régénération latent lors de leurs premiers stades de développement, un potentiel qui fluctue selon la réponse des cellules aux signaux de leur environnement direct.
Ces conclusions dessinent un horizon où la modification ciblée des voies de détection de l’oxygène pourrait améliorer de façon significative la cicatrisation humaine. Il convient toutefois de préciser que cette étude se concentre sur l’activation pure de mécanismes cellulaires, et non sur la capacité miraculeuse de recréer un bras ou une jambe dans sa totalité. L’idée d’une repousse imminente de membres humains relève de la méprise scientifique. Le véritable enseignement réside dans la preuve que des frontières biologiques jugées insurmontables entre les espèces sont en réalité modelées par l’environnement. « En comparant directement des espèces qui peuvent et ne peuvent pas régénérer, nous apportons une nouvelle perspective à une question vieille de plusieurs siècles. Nos résultats montrent que des programmes de régénération peuvent être déclenchés dans les tissus des mammifères et commencent à esquisser une voie claire et testable pour promouvoir la régénération des membres chez les mammifères adultes », a ajouté Aztekin.
Selon la source : iflscience.com