Une seule injection pour vaincre le cholestérol ? La science franchit un cap décisif (et risqué)
Auteur: Mathieu Gagnon
La fin de la pilule quotidienne ?

Imaginez un monde où la gestion du cholestérol ne dépendrait plus de cette petite pilule qu’il faut avaler chaque matin, sans faute, pour le restant de ses jours. C’est le pari un peu fou, mais fascinant, d’une nouvelle thérapie génique à dose unique. Une équipe de chercheurs, dirigée par le Dr Luke J. Laffin de la célèbre Cleveland Clinic, vient de tester une approche qui pourrait bien bousculer la cardiologie moderne. L’idée ? Modifier directement un gène dans le foie pour désactiver une protéine spécifique, l’ANGPTL3.
Les premiers résultats sont tombés, et ils sont assez spectaculaires pour qu’on s’y attarde, même si la prudence reste de mise. Si cette méthode s’avère durable et surtout sûre sur le long terme — ce qui reste à prouver —, elle pourrait redéfinir la façon dont des millions de personnes réduisent leurs risques de maladies cardiaques. C’est une promesse immense, mais qui ne laisse, avouons-le, que très peu de place à l’erreur.
Des résultats frappants teintés de prudence
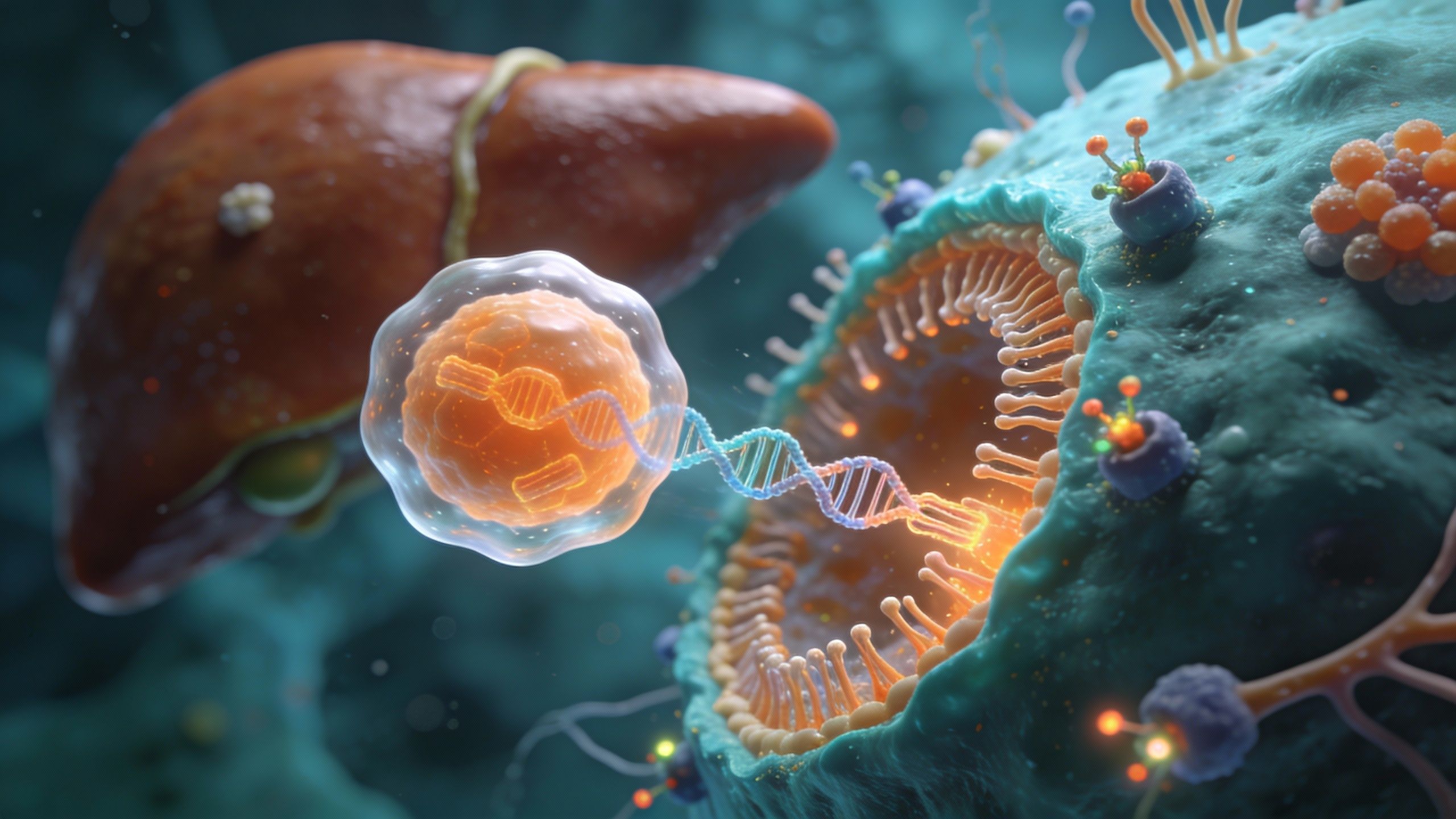
Alors, qu’est-ce que ça donne concrètement ? Lors de cet essai de phase un, 15 adultes ont reçu une injection unique. Les médecins les ont surveillés comme le lait sur le feu, c’est le moins qu’on puisse dire. Pour les quatre participants ayant reçu la dose la plus élevée, les chiffres sont éloquents : le cholestérol LDL — ce fameux « mauvais » gras qui encrasse les artères — a chuté de 48,9 %. Plus impressionnant encore, les triglycérides ont dégringolé de 55,2 % en l’espace de 60 jours. Pourquoi ? Parce que le traitement réduit l’ANGPTL3, une protéine hépatique qui freine normalement la dégradation des graisses. En la bloquant, les enzymes font le ménage beaucoup plus vite.
Mais attention, tout n’est pas rose. La médecine expérimentale est un terrain parfois brutal. Deux participants ont subi des événements graves, dont un décès soudain, et trois ont signalé des réactions à l’injection. Le Dr Laffin a noté qu’aucun effet toxique limitant la dose n’avait été directement lié au traitement CTX310 lui-même après examen, mais cela laisse planer une ombre. Un suivi à long terme est absolument crucial, car on ne joue pas avec l’ADN sans risques.
Le mécanisme est d’une complexité fascinante. Le traitement utilise des nanoparticules lipidiques — de minuscules transporteurs graisseux — pour livrer l’éditeur de gènes (CRISPR-Cas9) directement aux cellules du foie. Une fois à l’intérieur, la machinerie cellulaire lit les instructions, coupe l’ADN à un endroit précis et, en se réparant, désactive le gène ANGPTL3. C’est une mutation dite de « perte de fonction ». Contrairement à un médicament qui s’élimine, ici, le foie continue de copier cet ADN modifié à mesure que les cellules se divisent. C’est permanent.
La génétique comme source d’inspiration

Ce n’est pas sorti de nulle part. La génétique humaine nous avait déjà mis la puce à l’oreille. On sait que certaines personnes portent naturellement des mutations qui désactivent l’ANGPTL3, et devinez quoi ? Leurs artères sont en bien meilleur état. Une vaste analyse a montré que les porteurs de ces variantes bénéfiques avaient environ 34 % de risques en moins de développer une maladie coronarienne. L’objectif ici est de copier cet avantage naturel, même si intervenir tard dans la vie ne rattrapera jamais des décennies d’exposition réduite depuis la naissance.
Pour les patients qui jonglent déjà avec une montagne de médicaments sans atteindre leurs objectifs, ou pour ceux qui souffrent de troubles lipidiques héréditaires sévères, ce traitement pourrait être le Saint Graal. Il existe déjà une option, l’évinacumab, un anticorps qui bloque l’ANGPTL3, mais une édition génique unique réglerait le problème d’adhésion au traitement. On oublie souvent sa pilule, mais on ne peut pas oublier une modification de son propre ADN.
Conclusion : Entre espoir éthique et réalité clinique

Cependant, l’irréversibilité fait peur. Comme le corps ne peut pas annuler cette mutation, les médecins doivent être absolument certains de leur coup. Le Dr Laffin a précisé dans ses écrits : « Aucun effet toxique limitant la dose lié au CTX310 n’est survenu », mais la surveillance des marqueurs sanguins (les aminotransférases) pour détecter une inflammation hépatique devra durer des années.
Et puis, il y a la question de l’accès. En 2022, les maladies coronariennes ont causé 371 506 décès rien qu’aux États-Unis. La demande serait colossale. Si ce traitement arrive sur le marché, qui pourra se l’offrir ? Si seuls les systèmes de santé riches y ont accès, cela ne fera que creuser les inégalités déjà béantes. L’étude, publiée dans le New England Journal of Medicine, pose les premières pierres. Mais pour transformer l’essai, il faudra prouver que cette baisse du cholestérol réduit réellement les crises cardiaques et les AVC, sans provoquer de dégâts inattendus sur d’autres gènes. C’est un pari sur l’avenir, passionnant mais vertigineux.
Selon la source : earth.com
Ce contenu a été créé avec l’aide de l’IA.