Une créature marine a découvert le secret de l’immortalité — et les humains pourraient bien s’en inspirer
Auteur: Mathieu Gagnon
Des capacités de guérison qui humilient notre biologie

Soyons honnêtes : nous, les Homo sapiens, on se débrouille pas mal en matière de réparation. Une fracture ? L’os se ressoude. Une plaie ? La peau cicatrise. Certains de nos organes peuvent même repousser après une blessure dévastatrice. C’est impressionnant, certes, mais cela reste assez pâle comparé aux super-pouvoirs de l’anémone étoilée, ou Nematostella vectensis pour les intimes.
Cette petite créature marine ne joue tout simplement pas dans la même catégorie que nous. Alors que le règne animal regorge d’espèces aux capacités régénératrices remarquables, peu arrivent à la cheville des Cnidaires, ce groupe qui inclut les hydres, les méduses et les anémones de mer. Certaines, comme la méduse Turritopsis dohrnii, sont même fonctionnellement immortelles. Une étude récente publiée dans la revue Science Advances suggère que nous pourrions enfin comprendre comment elles font, et peut-être même nous en inspirer pour lutter contre les ravages du temps.
L’anémone qui refuse de vieillir
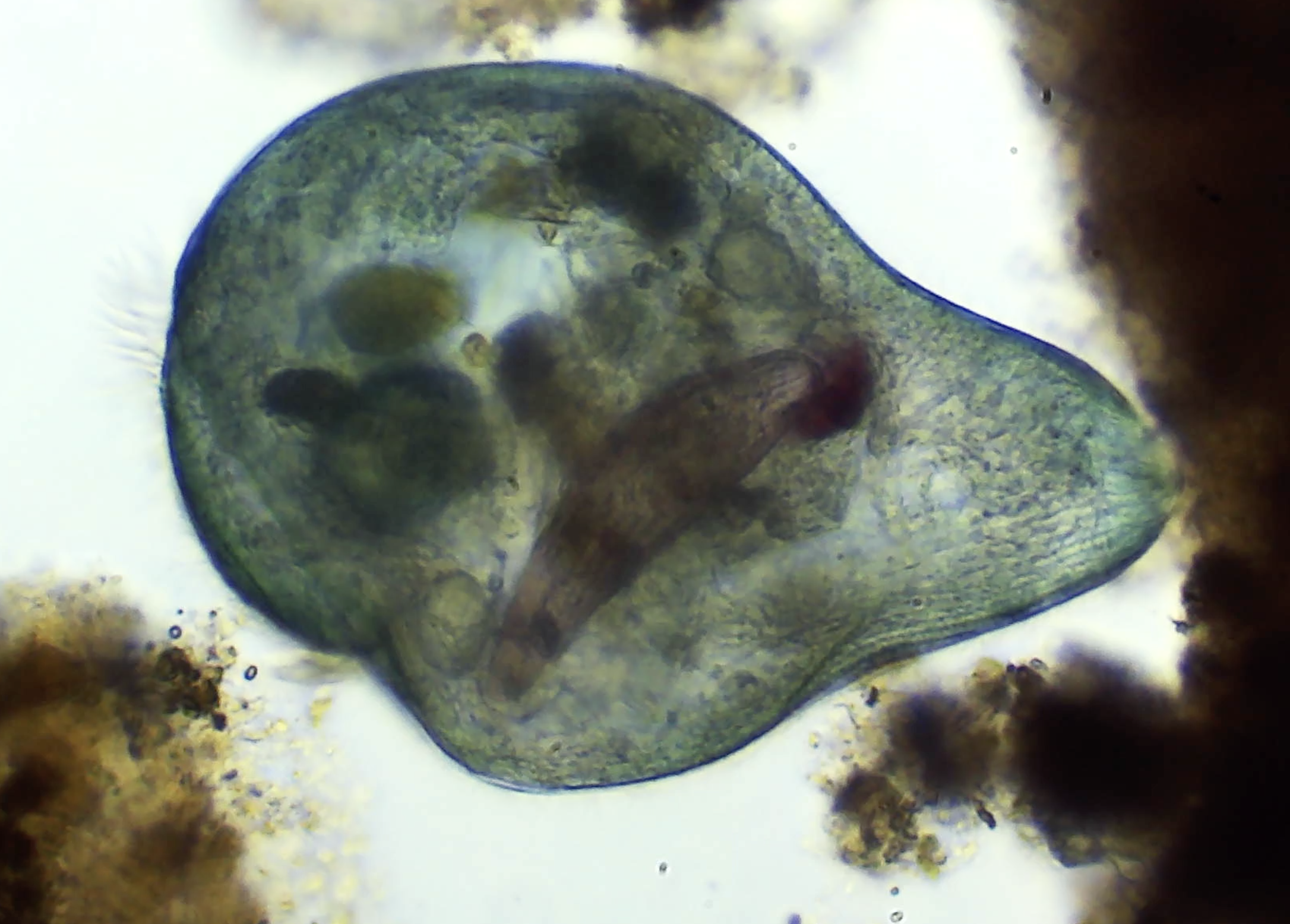
Mais qui est cette fameuse anémone étoilée ? Vous la trouverez principalement le long de la côte Est des États-Unis, avec quelques populations introduites sur la côte Ouest américaine et au sud-est de la Grande-Bretagne. Ce membre du phylum des Cnidaires est célèbre pour sa capacité à régénérer son corps entier. C’est cette faculté à défier, semble-t-il, le processus de vieillissement qui en fait une vedette de la recherche anti-âge.
Le problème, c’est que comprendre le « comment » s’est avéré un véritable casse-tête. La N. vectensis est pourtant l’organisme modèle idéal : elle se reproduit facilement en laboratoire (aussi bien de façon asexuée que sexuée) et ne montre pratiquement aucun signe de vieillesse. Mais jusqu’à présent, les scientifiques n’arrivaient pas à identifier les cellules souches responsables de cette jeunesse éternelle. La raison ? Elles sont d’une taille extrêmement réduite, ce qui les rendait presque invisibles à nos instruments.
La traque génétique porte enfin ses fruits

C’est là qu’interviennent les chercheurs de l’Université de Vienne. Sous la direction d’Ulrich Technau, l’auteur principal de l’étude, l’équipe a utilisé une nouvelle méthode appelée « génomique sur cellule unique » (single cell genomics) pour débusquer ces cellules manquantes. En gros, ils ont réussi à discerner la lignée des cellules souches en se basant sur les profils de transcriptome, qui sont une collection de transcrits d’ARNm.
Andreas Denner, le premier auteur de l’étude, explique cette avancée : « En combinant les analyses d’expression génique sur cellule unique et la transgénèse, nous avons pu identifier une large population de cellules chez l’anémone de mer qui forment des cellules différenciées, comme les cellules nerveuses et glandulaires ». Pour faire simple : ils ont trouvé des candidates très sérieuses au titre de cellules souches multipotentes. Ce sont elles qui permettraient aux Cnidaires de boire continuellement à la proverbiale fontaine de jouvence, là où nos propres cellules souches humaines ne permettent qu’une régénération limitée.
Un mécanisme vieux de 600 millions d’années
Pour valider leur découverte, l’équipe a zoomé sur deux gènes très spécifiques : nanos et piwi. Ce sont des gènes « hautement conservés », c’est-à-dire qu’ils n’ont pratiquement pas changé au cours de l’évolution. Ils codent pour des protéines régulatrices impliquées dans la différenciation des cellules souches et la gamétogenèse (le processus de création des spermatozoïdes et des ovules).
Les chercheurs ont alors utilisé les fameux ciseaux génétiques CRISPR pour muter le gène nanos2. Résultat ? Ils ont découvert que cette protéine est indispensable pour former non seulement les cellules germinales, mais aussi les cellules somatiques. Selon l’étude, ce mécanisme serait apparu dans la nature il y a environ 600 millions d’années. Maintenant que les scientifiques tiennent ces candidates cellules souches, les futures recherches vont pouvoir plonger plus profondément dans les mécanismes qui font des anémones d’aussi bons combattants contre le vieillissement. L’espoir, à terme, est de comprendre comment appliquer ces leçons biologiques à notre propre espèce.
Selon la source : popularmechanics.com
Créé par des humains, assisté par IA.