Hypertension : une découverte majeure relie le cerveau à l’hypertension artérielle
Auteur: Simon Kabbaj
Pour la plupart des personnes souffrant d’hypertension, le diagnostic s’accompagne d’une liste de causes bien connues : trop de sel, un manque d’exercice, une prise de poids ou encore le stress. Ces facteurs sont réels et leur gestion est essentielle. Pourtant, pour une part non négligeable de patients, le tensiomètre reste obstinément dans le rouge, même en suivant scrupuleusement toutes les recommandations : alimentation saine, prise de médicaments, réduction du sodium.
Cet écart tenace entre les solutions médicales actuelles et les besoins réels des patients frustre les cardiologues depuis longtemps. Une nouvelle piste de recherche pointe aujourd’hui vers une explication que peu avaient anticipée. Pour certains, l’origine du problème ne se trouverait ni dans le cœur, ni dans les reins, ni même dans les vaisseaux sanguins. Elle pourrait être logée dans le cerveau.
Plus précisément, la source se situerait dans une minuscule région du tronc cérébral, inconnue du grand public et que les scientifiques eux-mêmes n’associaient que très récemment à la pression artérielle. Bien que ces découvertes soient à un stade précoce, menées sur des animaux, leur portée est telle que les chercheurs en cardiovasculaire y prêtent une attention particulière. L’équipe à l’origine de ces travaux annonce même qu’une potentielle voie de traitement est déjà en cours de développement.
Un fléau mondial qui ne faiblit pas

L’hypertension est un problème de santé publique majeur, et son ampleur ne cesse de croître. Selon le Rapport mondial sur l’hypertension de l’OMS, publié en 2023, 1,4 milliard de personnes vivaient avec cette pathologie, mais à peine plus d’une sur cinq parvenait à la contrôler. Un chiffre alarmant : le nombre total de cas a doublé depuis 1990, et deux tiers des adultes concernés résident dans des pays à revenu faible ou intermédiaire.
Les conséquences sont graves. L’hypertension est l’une des principales causes d’infarctus, d’accident vasculaire cérébral (AVC), de maladie rénale chronique et de démence. Rien qu’aux États-Unis, une note d’information des CDC de 2024, basée sur l’enquête nationale sur la santé et la nutrition, a révélé que près de 47,7 % des adultes américains remplissent les critères de l’hypertension artérielle.
Les traitements actuels, qui incluent des médicaments comme les inhibiteurs de l’ECA, les inhibiteurs calciques et les bêta-bloquants, ainsi que des changements de mode de vie, sont efficaces pour beaucoup. Cependant, un pourcentage significatif de patients n’y répond pas suffisamment. L’hypertension initiée et maintenue par le cerveau est définie comme une hypertension neurogène ; elle représente près de la moitié de tous les cas. Une part importante de ces individus hypertendus restent non contrôlés malgré le traitement, et cette population a tendance à présenter des niveaux élevés ou inappropriés d’activité nerveuse sympathique. C’est précisément cette composante neurologique que la nouvelle recherche a voulu explorer.
Au cœur du cerveau : une région au double jeu
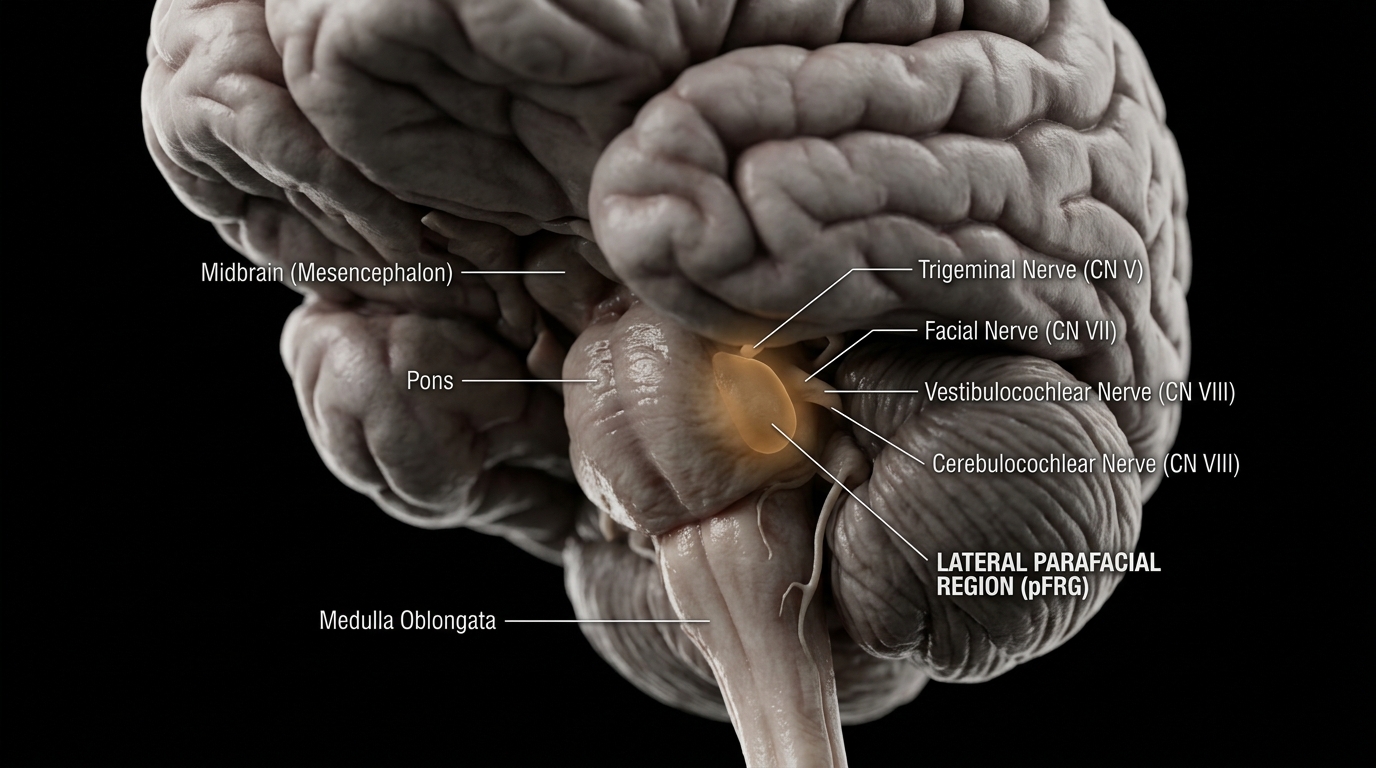
La région en question, appelée région parafaciale latérale (pFL), est située dans le tronc cérébral, la partie la plus ancienne de notre cerveau qui contrôle les fonctions automatiques comme la digestion, la respiration et le rythme cardiaque. Avant ces recherches, cette zone était principalement connue pour son rôle dans un type de respiration très spécifique. Comme l’explique le chercheur principal, le professeur Julian Paton, directeur du Manaaki Manawa, Centre de recherche sur le cœur à l‘Université d’Auckland : « La région parafaciale latérale est mise en action pour nous faire expirer lors d’un rire, d’un exercice ou d’une toux. Ces expirations sont ce que nous appelons ‘forcées’ et sont entraînées par nos puissants muscles abdominaux. En revanche, une expiration normale n’a pas besoin que ces muscles se contractent – elle se produit parce que les poumons sont élastiques. »
Ce que l’équipe de recherche a découvert, c’est que cette région liée à la respiration possède une seconde fonction, aux conséquences bien plus vastes. Les scientifiques ont constaté que cette zone se connecte également à des nerfs qui resserrent les vaisseaux sanguins, un mécanisme qui fait monter la pression artérielle. Autrement dit, une région que le corps utilise pour déclencher un rire ou une toux a aussi la capacité de comprimer les vaisseaux et d’augmenter la pression dans nos artères.
L'expérience qui a tout changé
Pour vérifier leur hypothèse, les chercheurs ont mené des expériences sur des rats. À l’aide de techniques de génie génétique, ils ont pu « allumer » ou « éteindre » les neurones de la région pFL, puis observer les effets. L’activité nerveuse liée à la respiration, l’activité nerveuse sympathique et la pression artérielle étaient toutes surveillées. Lorsque l’équipe a activé les neurones pFL chez certains rats, cela a déclenché d’autres circuits cérébraux qui ont finalement fait grimper la pression artérielle des animaux. Ils ont ensuite cartographié en détail l’activité du tronc cérébral et des nerfs, y compris les autres neurones avec lesquels la région pFL communiquait, et ont comparé les données avec celles de rats témoins non hypertendus.
Le résultat, lorsque le processus a été inversé, fut tout aussi frappant. « Nous avons découvert que, dans des conditions d’hypertension, la région parafaciale latérale est activée et, lorsque notre équipe a inactivé cette région, la pression artérielle est revenue à des niveaux normaux », rapporte le professeur Paton.
Chez les rats hypertendus, les neurones pFL n’aidaient pas seulement à la respiration : ils agissaient également pour contracter les vaisseaux sanguins. Ce double rôle, à la fois dans le réseau respiratoire et dans le réseau de régulation vasculaire, n’avait jamais été identifié auparavant. Cette découverte suggère que des changements dans les schémas respiratoires, en particulier ceux impliquant de fortes contractions des muscles abdominaux, pourraient déclencher une pression artérielle élevée. Identifier une respiration abdominale anormale chez les patients hypertendus pourrait ainsi orienter vers la cause et un traitement plus approprié.
Le lien entre respiration et tension artérielle
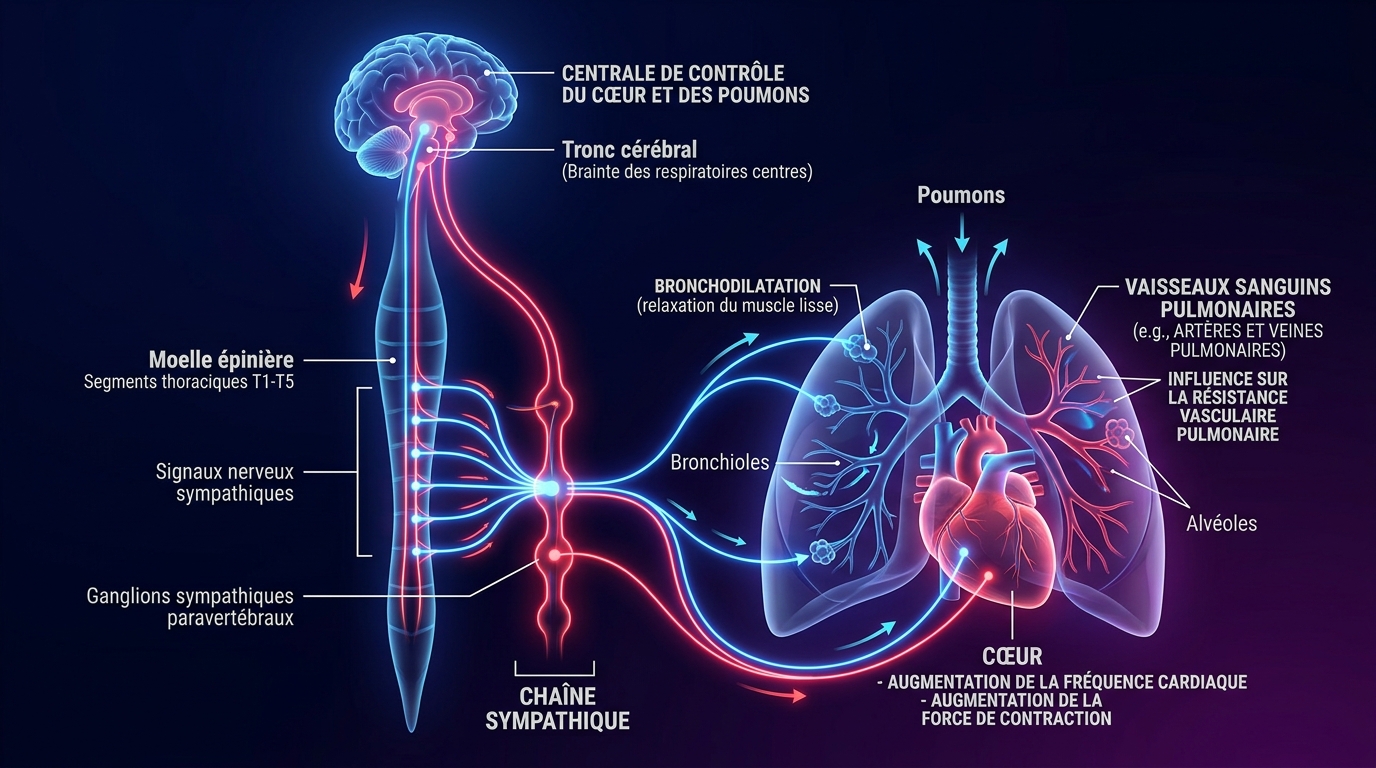
L’étude suggère que les neurones pFL pourraient relier les changements de rythme respiratoire à une activité accrue du système nerveux sympathique, la réponse de « combat ou de fuite » de l’organisme, qui aide à contrôler la pression artérielle. Cela corrobore des recherches antérieures liant l’hypertension au cerveau et au système nerveux. Lorsque le système sympathique est suractivé de manière chronique, les vaisseaux sanguins restent contractés et le cœur travaille plus fort, ce qui entraîne une hypertension artérielle durable.
Les recherches menées au cours des trois dernières décennies sur des patients atteints d’hypertension essentielle ont établi un consensus : une activité sympathique dirigée vers la vascularisation des muscles squelettiques, le cœur et les reins est activée chez 40 à 65 % des patients. Cet ensemble de preuves bien établies donne un poids supplémentaire aux nouvelles découvertes. La région parafaciale latérale pourrait être l’une des sources en amont qui alimentent cette suractivité sympathique chronique.
Hypertension neurogène : une pièce manquante du puzzle

Le concept d’hypertension neurogène – une pression artérielle élevée principalement par l’activité du système nerveux plutôt que par des facteurs périphériques comme la fonction rénale ou le volume de fluides – n’est pas nouveau. Une composante neurogène dans l’hypertension primaire est aujourd’hui bien établie, et l’activation chronique du système nerveux sympathique dans ce contexte produit diverses conséquences physiopathologiques, indépendamment de toute augmentation de la pression artérielle elle-même.
Ce qui restait insaisissable, c’était un mécanisme clair et ciblable. Identifier les circuits cérébraux qui génèrent l’excès de signaux sympathiques a été un défi constant. Comme l’écrivent les chercheurs dans leur article publié : « Étant donné qu’environ 50 pour cent des patients hypertendus ont une composante neurogène, le défi est de comprendre les mécanismes générant la sympatho-excitation dans l’hypertension. Une telle révélation fournirait une orientation clinique indispensable pour de nouvelles stratégies thérapeutiques. »
La région parafaciale latérale pourrait être une pièce de ce puzzle. Selon les mots de Julian Paton : « Nous avons mis au jour une nouvelle région du cerveau qui cause l’hypertension artérielle. Oui, le cerveau est à blâmer pour l’hypertension ! » Pour ceux qui suivent des patients atteints d’hypertension résistante au traitement ou inexpliquée, ce cadre est cliniquement pertinent. L’hypertension neurogène est plus probable chez les patients présentant une hypertension labile ou paroxystique (soudaine, en courtes poussées), mais des preuves d’un tonus sympathique accru pointent également vers une composante neurogène chez les patients atteints d’hypertension sévère ou résistante, de maladie rénale chronique et de comorbidités associées.
L'apnée du sommeil : un éclairage nouveau

L’un des aspects les plus immédiatement pratiques de cette recherche concerne l’apnée du sommeil, un trouble où la respiration s’arrête et reprend de manière répétée pendant le sommeil. Une recherche publiée en 2024 dans Hypertension Research a confirmé que l’apnée obstructive du sommeil et l’hypertension ont un taux de co-occurrence élevé, l’apnée du sommeil agissant comme un facteur causal de l’hypertension. L’activité sympathique provoquée par l’hypoxie intermittente est l’un des mécanismes les plus importants déclenchant l’élévation de la pression artérielle dans ce contexte.
Les nouvelles découvertes offrent une explication neurologique plausible à ce lien. Alors que les neurones pFL ne sont pas impliqués dans la respiration normale, ils s’activent en réponse à des niveaux élevés de CO2 ou faibles d’oxygène – précisément ce qui se passe pendant l’apnée du sommeil. Lorsque la respiration s’arrête de façon répétée pendant la nuit, les niveaux d’oxygène chutent et le dioxyde de carbone s’accumule. Ce changement chimique active la région pFL qui, à son tour, active le système sympathique, resserre les vaisseaux sanguins et fait monter la pression artérielle.
Cela pourrait expliquer pourquoi l’hypertension chez les patients souffrant d’apnée du sommeil peut persister même pendant les heures d’éveil. Une recherche publiée dans Clinical Hypertension en 2024 a noté que la suractivation du système sympathique lors d’épisodes répétés d’apnée entraîne des pics de pression artérielle épisodiques, et que cette voie est un mécanisme central reliant les deux conditions. Pour les lecteurs qui ont à la fois un diagnostic d’hypertension et des troubles respiratoires du sommeil, cette convergence de découvertes mérite d’être discutée avec un médecin, surtout si la pression artérielle reste difficile à contrôler.
Une cible thérapeutique inattendue dans le cou
L’aspect le plus significatif de cette nouvelle recherche réside peut-être dans la piste de traitement qu’elle ouvre. Les chercheurs ont reconnu un problème central dès le départ : même si la région pFL est un moteur de l’hypertension, il est extraordinairement difficile de faire agir des médicaments sur une zone aussi petite et spécifique du cerveau sans affecter les tissus environnants. « Cibler le cerveau avec des médicaments est délicat car ils agissent sur tout le cerveau et non sur une région sélectionnée comme le noyau parafacial », explique le professeur Paton.
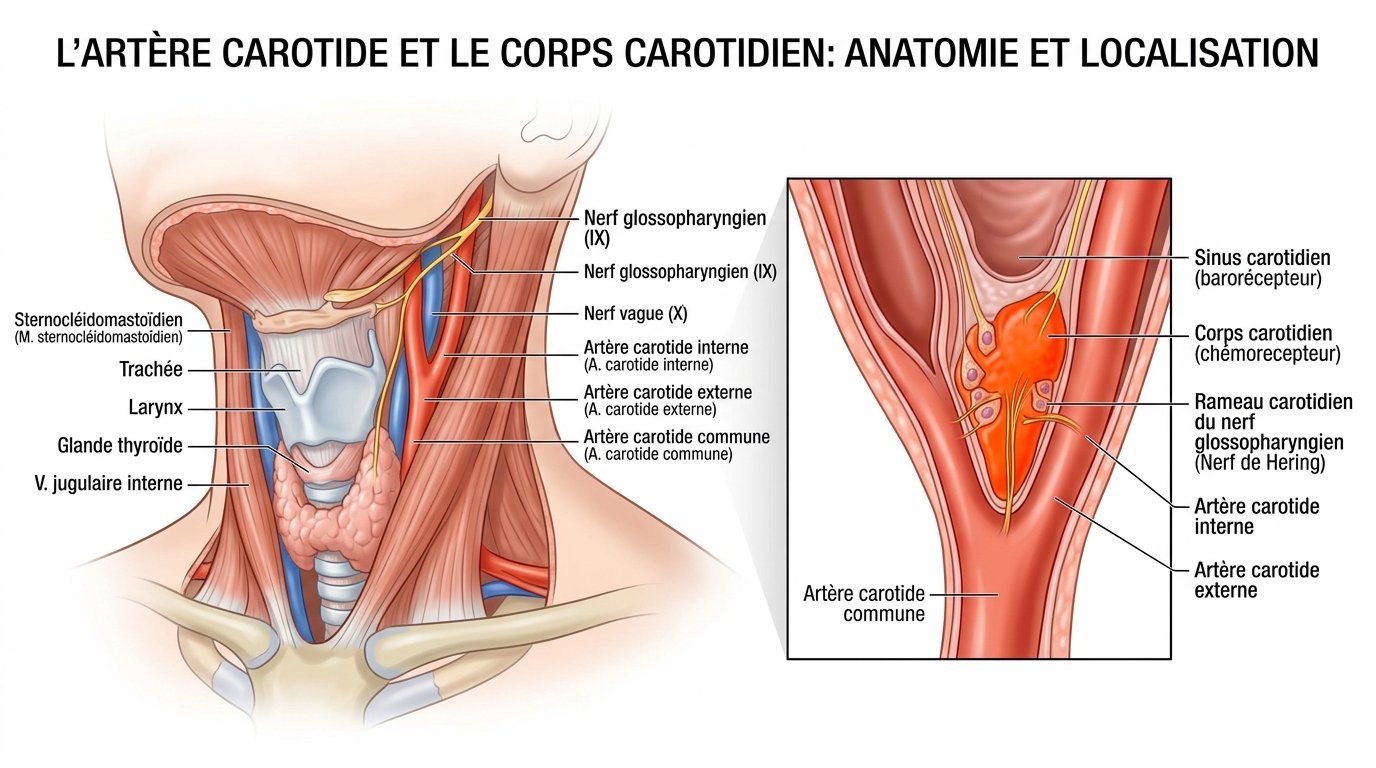
La percée est venue lorsque l’équipe a retracé les signaux qui activaient la région pFL. Ils ont découvert que cette région est activée par des signaux provenant de l’extérieur du cerveau, émis par les glomus carotidiens (ou corpuscules carotidiens). Ce sont de minuscules amas de cellules situés dans le cou, près de l’artère carotide, qui détectent les niveaux d’oxygène dans le sang. Parce qu’ils se trouvent à l’extérieur de la barrière hémato-encéphalique, ces capteurs peuvent être ciblés par des médicaments de manière beaucoup plus sûre que le tissu cérébral lui-même.
Les glomus carotidiens ne sont pas un concept nouveau dans la recherche sur l’hypertension. Des chercheurs de l’Université de Bristol avaient déjà découvert qu’ils semblaient être une cause d’hypertension, et leur équipe clinique a démontré que le retrait d’un glomus carotidien chez certains patients atteints d’hypertension résistante entraînait une baisse immédiate et durable de la pression artérielle. La nouvelle étude ajoute le chaînon manquant : le lien mécanique. Les glomus carotidiens semblent être en amont de la région parafaciale latérale. En « calmant » les glomus carotidiens, les chercheurs pourraient être en mesure de réduire l’activité de la pFL sans jamais toucher directement au cerveau. « Notre objectif est de cibler les glomus carotidiens, et nous importons un nouveau médicament que nous réutilisons pour calmer leur activité et inactiver ‘à distance’ la région parafaciale latérale en toute sécurité, c’est-à-dire sans avoir besoin d’un médicament qui pénètre dans le cerveau », précise Julian Paton.
Prudence et perspectives : où en est la science ?

Toute lecture responsable de cette recherche doit prendre ses limites au sérieux. L’étude n’a utilisé que des modèles animaux. Il est probable, mais pas certain, que les mêmes circuits existent chez l’homme. La physiologie des rats et celle des humains partagent de nombreuses caractéristiques, mais elles ne sont pas identiques. Ce qui fonctionne dans une expérience contrôlée sur des animaux ne se traduit pas automatiquement dans un environnement clinique humain complexe.
Le chemin d’un modèle de rat à un essai clinique sur l’homme est long, coûteux et se solde souvent sans le résultat escompté. L’histoire des neurosciences et de la médecine cardiovasculaire est remplie de découvertes précliniques prometteuses qui n’ont pas survécu à des tests rigoureux sur l’homme.
De plus, l’hypertension neurogène n’est presque certainement pas une condition unique et uniforme. La cause principale de la plupart des cas d’hypertension reste floue, et même parmi ceux ayant une composante neurogène claire, les mécanismes spécifiques peuvent différer d’une personne à l’autre. La région parafaciale latérale peut être un contributeur significatif pour certains patients, en particulier ceux avec des schémas respiratoires anormaux ou une apnée du sommeil, tout en étant beaucoup moins pertinente pour d’autres dont l’hypertension est due à des voies différentes. Ce que cette étude accomplit, même en tenant compte de ces limites, c’est d’ouvrir une hypothèse spécifique et testable. Une question bien définie à laquelle la recherche humaine peut maintenant commencer à répondre.
Un nouvel espoir pour l'hypertension résistante ?

L’hypertension résistante, définie comme une pression artérielle qui reste élevée malgré la prise de trois médicaments antihypertenseurs ou plus à des doses appropriées, est un défi clinique majeur. Les patients atteints de véritable hypertension résistante se caractérisent par une activité sympathique élevée, ce qui en fait des candidats pour des traitements visant à réduire l’activité du système nerveux sympathique.
Les approches existantes basées sur des dispositifs, telles que la dénervation rénale (ablation des nerfs sympathiques autour des reins) et la thérapie d’activation du baroréflexe carotidien (stimulation électrique des capteurs de pression dans le cou), ont montré des résultats variables dans les essais cliniques. Des preuves croissantes ont confirmé le potentiel de l’amplification du baroréflexe pour améliorer le contrôle de la pression artérielle chez ces patients, avec un profil d’effets secondaires limité. Mais aucune approche ne s’est avérée universellement efficace, renforçant l’idée que l’hypertension résistante est hétérogène dans ses origines.
La voie de la pFL représente un mécanisme distinct que les thérapies actuelles ne ciblent pas spécifiquement. Si des études humaines confirment qu’une suractivité des neurones pFL contribue à l’hypertension résistante chez une proportion significative de patients, l’approche médicamenteuse ciblant le glomus carotidien pourrait à terme offrir une nouvelle option. Précisément pour ces patients qui ont épuisé les choix conventionnels. Le mot clé, cependant, est « si ». Il s’agit à ce stade d’une science génératrice d’hypothèses, pas d’un traitement prouvé.
Ce que cette découverte signifie pour vous

Cette recherche, publiée dans la revue Circulation Research fin 2025, marque une avancée significative dans la compréhension des raisons pour lesquelles l’hypertension est si difficile à traiter chez une minorité substantielle de patients. La conclusion principale est qu’une petite région du tronc cérébral, la zone parafaciale latérale, peut agir comme un moteur de l’hypertension en activant les nerfs qui contractent les vaisseaux sanguins. Ce mécanisme semble fonctionner via le système nerveux sympathique, le même réseau de « combat ou de fuite » longtemps impliqué dans l’hypertension neurogène.
La connexion avec les glomus carotidiens est particulièrement importante du point de vue du traitement. Ces minuscules structures de détection d’oxygène dans le cou semblent activer la région pFL et se situent à l’extérieur de la barrière hémato-encéphalique, ce qui les rend plus accessibles à une intervention pharmacologique que le tissu cérébral lui-même. Un médicament réadapté, conçu pour supprimer l’activité des glomus carotidiens sans entrer dans le cerveau, est déjà en cours de développement par l’équipe de recherche.
Pour les personnes qui gèrent actuellement leur hypertension avec des médicaments, rien dans cette étude ne modifie les recommandations cliniques aujourd’hui. Les thérapies antihypertensives standards, la surveillance régulière de la pression artérielle, la réduction du sel dans l’alimentation, l’activité physique et la qualité du sommeil restent les pierres angulaires de la prise en charge. Pour celles souffrant d’hypertension résistante ou inexpliquée, en particulier si des troubles respiratoires du sommeil sont également présents, la compréhension émergente des voies neurogènes pourrait à terme éclairer une approche plus ciblée de leurs soins. Demander à votre médecin si une composante neurogène pourrait contribuer à des lectures difficiles à contrôler est une conversation raisonnable à entamer, même maintenant.
Selon la source : sciencedaily.com
Créé par des humains, assisté par IA.