Un nouvel espoir contre les AVC : une injection post-crise pour protéger le cerveau
Auteur: Mathieu Gagnon
Le paradoxe cruel du traitement de l’AVC
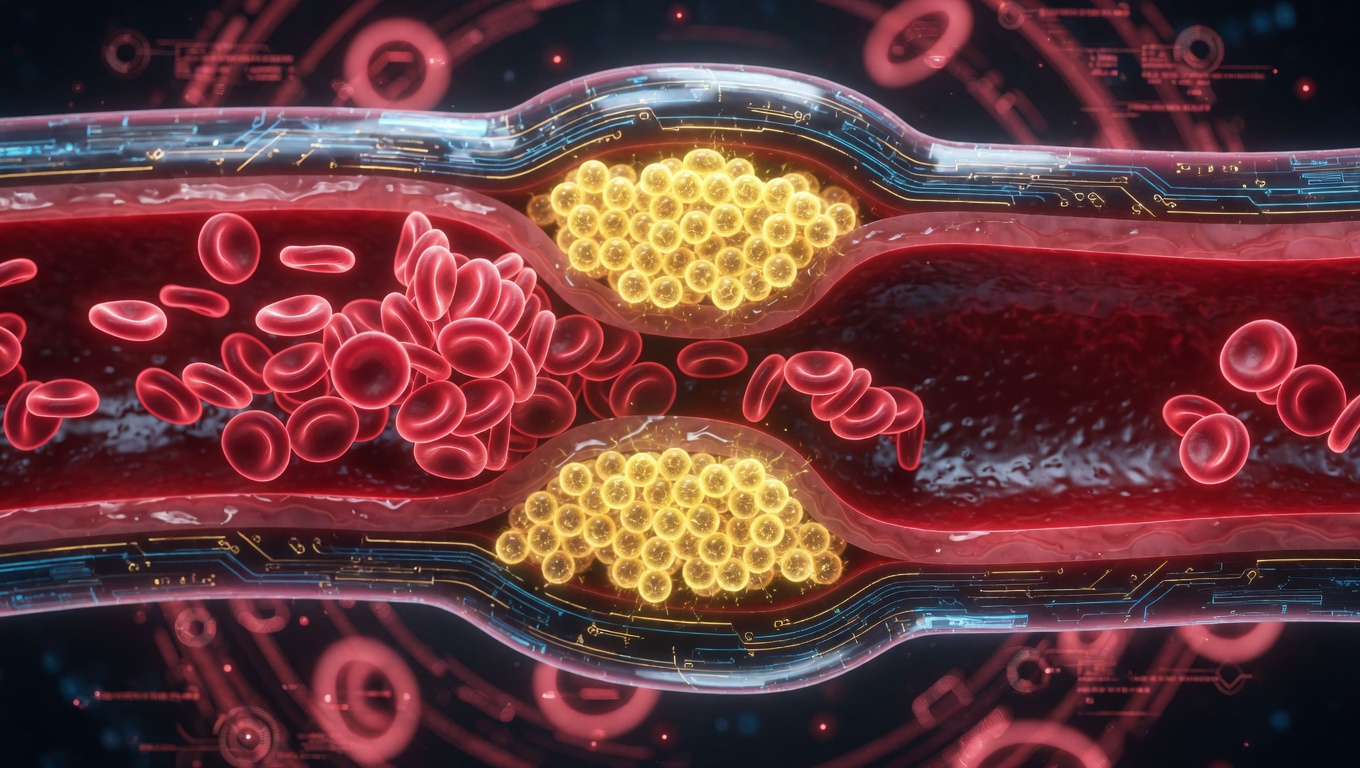
C’est une situation d’une ironie presque tragique, vous ne trouvez pas ? Lorsqu’une personne est frappée par un accident vasculaire cérébral (AVC), la priorité absolue des médecins est de rétablir le flux sanguin vers le cerveau le plus vite possible. C’est une question de vie ou de mort, littéralement. Mais voilà, ce retour brutal du sang, aussi vital soit-il, peut déclencher ce qu’on appelle une « seconde vague » de dommages. Cela semble contre-intuitif, mais cet afflux peut tuer des cellules cérébrales supplémentaires, alimenter l’inflammation et augmenter considérablement les risques de handicap à long terme.
Cependant, une lueur d’espoir nous vient de l’Université Northwestern. Des scientifiques y ont développé un nanomatériau régénératif injectable, conçu spécifiquement pour intervenir durant cette fenêtre de vulnérabilité. Dans une nouvelle étude préclinique publiée dans la revue Neurotherapeutics, intitulée « Toward Development of a Dynamic Supramolecular Peptide Therapy for Acute Ischemic Stroke », l’équipe a administré une dose intraveineuse unique juste après avoir rétabli le flux sanguin sur un modèle de souris.
Les résultats sont, disons-le, assez stupéfiants. La thérapie a réussi à franchir la barrière hémato-encéphalique — ce qui est un défi colossal pour la plupart des médicaments — pour atteindre et réparer le tissu cérébral. Le Dr Ayush Batra, co-auteur correspondant et professeur associé en neurologie à la Northwestern University Feinberg School of Medicine, a d’ailleurs souligné que si les approches actuelles se concentrent uniquement sur la restauration du flux, il n’existe pas encore de traitement favorisant la récupération neuronale. Il a qualifié une telle thérapie de « Saint Graal » qui n’existe pas encore, tout en affirmant que cette étude nous met sur la bonne voie pour combler ce besoin non satisfait.
Les « molécules dansantes » : une technologie adaptable

Le secret de cette avancée réside dans ce que l’on appelle les peptides thérapeutiques supramoléculaires (STP). C’est une plateforme développée par Samuel I. Stupp, également de Northwestern. Pour la petite histoire, une étude publiée en 2021 dans la célèbre revue Science avait déjà démontré l’efficacité de cette technologie, surnommée les « molécules dansantes ». Pourquoi ce nom ? En raison de la nature hautement dynamique de ses agents thérapeutiques. À l’époque, une seule injection avait permis d’inverser la paralysie et de réparer les tissus chez des souris souffrant de graves lésions de la moelle épinière.
Ce qui est fascinant ici, c’est l’adaptation de cette technologie. Le secret derrière ces « molécules dansantes » est la capacité de régler le mouvement collectif des molécules pour qu’elles puissent trouver et engager correctement les récepteurs cellulaires, qui sont eux-mêmes en mouvement constant. Le traitement envoie des signaux qui encouragent les cellules nerveuses à se réparer elles-mêmes. Par exemple, cela peut aider les fibres nerveuses, les axones, à repousser et à se reconnecter, un processus connu sous le nom de plasticité.
Dans les études précédentes sur la moelle épinière, le liquide se transformait immédiatement en gel. Mais pour l’AVC, les scientifiques ont dû être plus malins. Ils ont réduit la concentration des assemblages peptidiques pour éviter la formation de caillots dans le sang. Samuel Stupp explique que de plus petits agrégats de peptides traversent plus facilement la barrière hémato-encéphalique. Une fois qu’ils sont passés en nombre suffisant, ils peuvent former de plus grands assemblages de nanofibres dans le tissu cérébral pour produire un effet thérapeutique puissant. C’est une prouesse d’ingénierie moléculaire qui permet une administration intraveineuse sans chirurgie invasive.
Des résultats prometteurs face à la réalité de l’AVC
Il faut bien se rendre compte de l’enjeu : l’AVC ischémique aigu représente environ 80 % de tous les AVC aux États-Unis. C’est une cause majeure de morbidité et de mortalité dans le monde. Le Dr Batra rappelle souvent que les AVC graves peuvent entraîner un handicap permanent, affectant non seulement la qualité de vie du patient, mais imposant aussi un lourd fardeau émotionnel et financier aux familles. Actuellement, les médecins utilisent des médicaments pour dissoudre les caillots ou des dispositifs pour les retirer chirurgicalement, mais cela ne répare pas les dommages déjà causés.
L’étude a cherché à imiter fidèlement la réalité clinique. Les chercheurs ont bloqué le flux sanguin chez les souris pour simuler un AVC majeur, puis l’ont rétabli (reperfusion), exactement comme le font les médecins aux urgences. Ils ont ensuite surveillé les souris pendant sept jours. Le constat est sans appel : aucun effet secondaire significatif, pas de toxicité organique ni de rejet immunitaire.
Grâce à des techniques d’imagerie avancées, comme la microscopie intravitale intracrânienne en temps réel, ils ont vu la thérapie se localiser sur le site de la lésion. Comparées aux souris non traitées, celles ayant reçu les « molécules dansantes » présentaient nettement moins de dommages aux tissus cérébraux. Samuel Stupp précise que la thérapie possède des propriétés à la fois pro-régénératrices et anti-inflammatoires. En gros, quand on retire le caillot, des « mauvais acteurs » (molécules nocives) sont libérés et causent des dégâts ; les molécules dansantes contrent ces effets tout en aidant à réparer les réseaux neuronaux.
Conclusion : Vers une application clinique ?

Ce qui a longtemps tourmenté le domaine des neurosciences, c’est le fait que des thérapies apparemment efficaces ne parvenaient tout simplement pas à traverser la barrière hémato-encéphalique. Cette nouvelle approche pourrait changer la donne. Le Dr Batra explique que lorsque le flux sanguin est rétabli, la perméabilité de cette barrière augmente localement et temporairement, créant une fenêtre d’opportunité. En y ajoutant un peptide dynamique capable de traverser plus facilement, on optimise les chances que le traitement arrive à bon port.
Bien sûr, il reste du chemin à parcourir. Les prochaines études devront évaluer si ce traitement peut soutenir une récupération fonctionnelle à plus long terme. On sait que de nombreux patients souffrent d’un déclin cognitif important dans l’année qui suit un AVC. L’équipe souhaite également tester si des signaux régénératifs supplémentaires pourraient être incorporés pour obtenir des résultats encore meilleurs.
Il convient de saluer le travail de toute l’équipe, y compris l’étudiant diplômé Zijun Gao et la chercheuse postdoctorale Luisa Andrade da Silva, qui sont co-premiers auteurs de ce papier. C’est une avancée qui, si elle se confirme, pourrait transformer la vie de millions de personnes.
Selon la source : medicalxpress.com
Ce contenu a été créé avec l’aide de l’IA.