Des chercheurs identifient une piste pour bloquer les signaux d’anxiété dans le cerveau
Auteur: Simon Kabbaj
Une découverte majeure dans le cerveau des souris
Le système d’alarme de notre cerveau est essentiel. Il identifie les menaces, mobilise notre attention et prépare le corps à l’action. Mais il arrive que ce même système se bloque en état d’alerte permanent, notamment après un stress intense. Depuis des années, les scientifiques tentent de comprendre pourquoi certains cerveaux récupèrent après une épreuve, tandis que d’autres continuent de sonner l’alarme. Une étude publiée dans Nature Communications et menée par Mariusz Mucha et ses collègues apporte une réponse saisissante.
Leurs travaux mettent en lumière une petite molécule d’ARN, localisée dans l’amygdale, qui semble capable d’atténuer certains effets néfastes du stress et de réduire les comportements anxieux chez les souris mâles. Si l’idée d’un interrupteur pour ‘éteindre’ l’anxiété fait un titre accrocheur, la réalité scientifique est plus précise et encore plus solide. L’équipe de l’Université de Bristol n’a pas montré que l’anxiété pouvait être effacée comme une lumière.
Ce qu’ils ont démontré est une chaîne biologique rigoureuse : un stress aigu a augmenté l’expression d’un microARN appelé miR-483-5p dans l’amygdale basolatérale. Cette molécule a ensuite supprimé l’expression du gène Pgap2. Enfin, l’ensemble de ce processus a été associé à une diminution des comportements de type anxieux lors de tests reconnus sur les souris. Dans un domaine où les affirmations excessives sont fréquentes, cette séquence biologique étroitement liée donne un poids considérable à la découverte et offre aux chercheurs une piste spécifique à explorer pour de futurs traitements.
À la recherche du ‘frein’ naturel du cerveau
Les troubles anxieux ne sont ni un problème médical marginal, ni un fardeau léger pour ceux qui en souffrent. Selon l’Organisation Mondiale de la Santé, 359 millions de personnes dans le monde étaient atteintes d’un trouble anxieux en 2021. L’OMS rapporte également que seulement 27,6 % des personnes ayant besoin de soins reçoivent un traitement. Ces chiffres expliquent la persévérance des chercheurs dans leur quête de meilleures cibles biologiques. Si les médicaments existants aident de nombreux patients, trop de personnes ne parviennent pas à une rémission complète. Un communiqué de presse de l’Université de Bristol indique même que plus de la moitié des patients n’atteignent pas la rémission avec les traitements anti-anxiété actuels.
C’est ce constat qui a guidé la logique de l’étude menée par l’équipe de Mariusz Mucha. Leur objectif était d’identifier les événements moléculaires se produisant à l’intérieur de l’amygdale qui influencent la réponse au stress. L’amygdale est une région clé, car elle se situe au centre du traitement de la peur et de l’apprentissage des menaces. Lorsqu’un stress devient intense ou prolongé, des changements peuvent s’y produire, favorisant des comportements anxieux durables. Les chercheurs de Bristol expliquent que les traumatismes peuvent déclencher des modifications génétiques, biochimiques et morphologiques dans les neurones de l’amygdale. C’est en cartographiant plus clairement cette biologie que l’on peut espérer développer des médicaments efficaces.
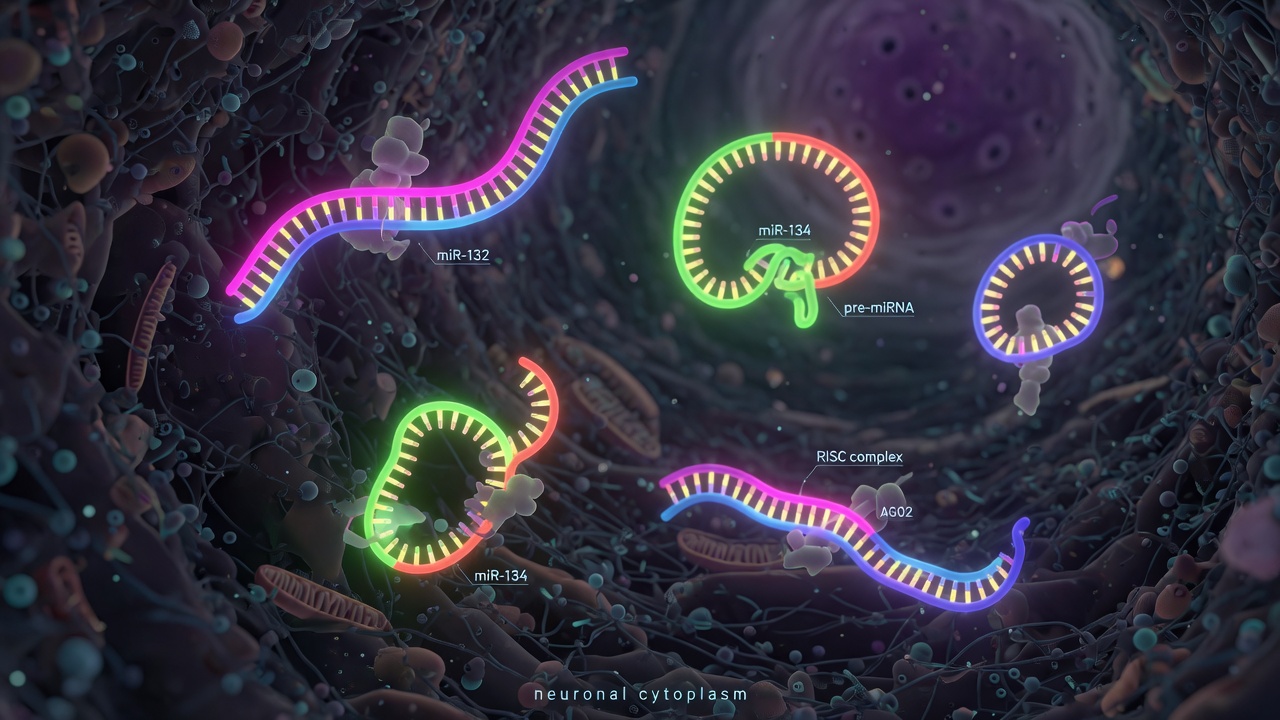
Les auteurs de l’étude ne cherchaient pas seulement des marqueurs du stress ; ils voulaient identifier des molécules qui pourraient activement aider à réduire l’anxiété après l’exposition. Le NIMH (National Institute of Mental Health) note que les troubles anxieux résultent d’influences à la fois environnementales et génétiques. Ce contexte rend les régulateurs de gènes, comme les microARNs, particulièrement intéressants. Ces derniers sont de petites molécules d’ARN non codantes qui régulent l’expression des gènes après leur transcription. Ils intéressent les neuroscientifiques car ils peuvent influencer simultanément des groupes entiers de gènes cibles, ce qui les rend adaptés à l’étude de conditions neuropsychiatriques complexes comme l’anxiété pathologique.
La piste révélatrice de la molécule miR-483-5p
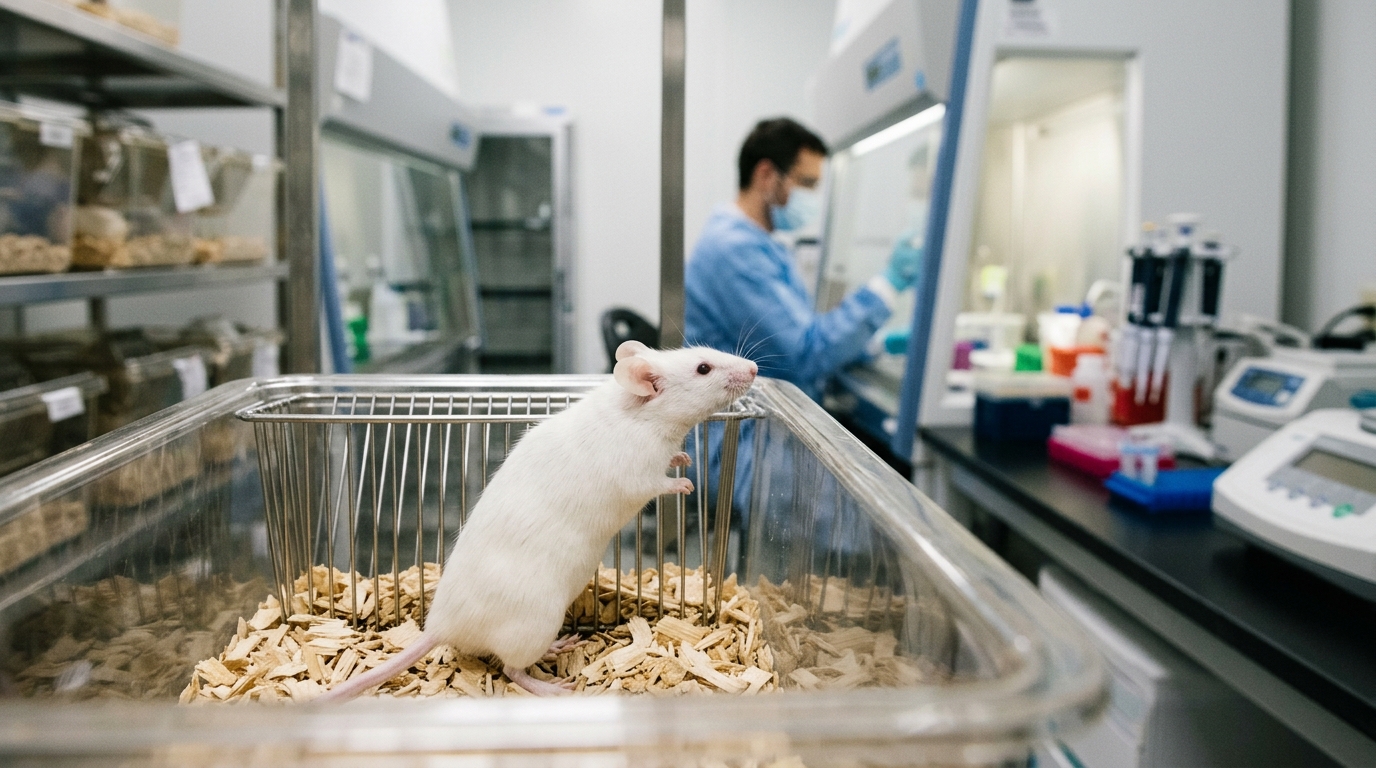
Pour leur étude, les chercheurs des universités de Bristol et d’Exeter ont utilisé des souris mâles adultes de la souche C57BL/6J. Ces animaux ont été soumis à un stress par contention de 6 heures. L’équipe a ensuite isolé du tissu de l’amygdale basolatérale pour l’analyser. Grâce à des tests par microréseaux, ils ont identifié les microARNs réagissant au stress dans cette région du cerveau. Un candidat s’est démarqué des autres : le miR-483-5p, dont le niveau augmentait après le stress et qui est devenu le point central de leurs travaux.
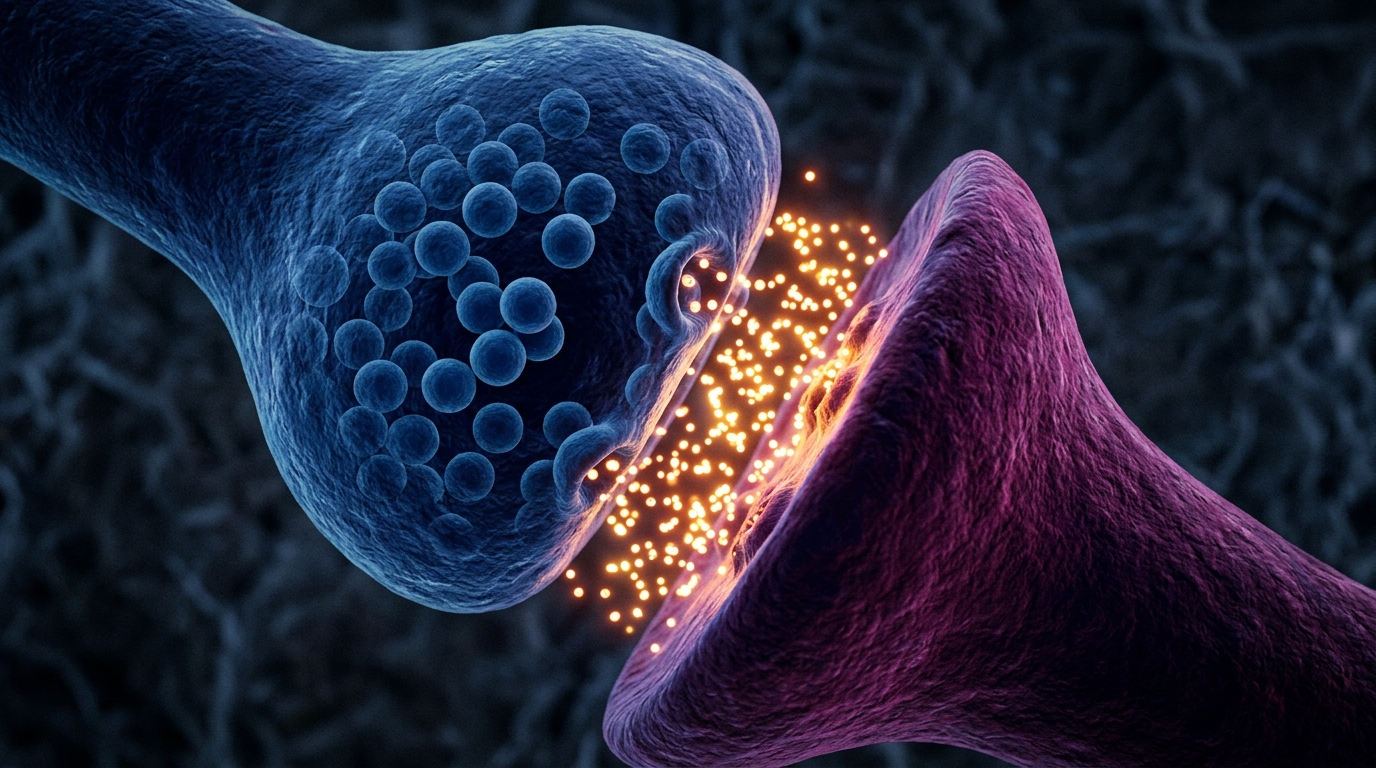
Les scientifiques ne se sont pas arrêtés à ce résultat général. Ils ont cherché où cette molécule apparaissait précisément. Ils l’ont trouvée principalement dans les neurones, et plus spécifiquement dans un sous-ensemble de synapses. L’équipe a ensuite mesuré un enrichissement quatre fois plus important du miR-483-5p dans la fraction synaptosomale, comparée à la fraction cytosolique chez des souris n’ayant pas subi de stress. Ce détail donne une profondeur et une crédibilité accrues à l’étude. Les synapses sont les points de contact où les neurones échangent des signaux, renforcent des circuits et encodent l’apprentissage émotionnel.
Une molécule réactive au stress qui se concentre à cet endroit précis peut faire bien plus que modifier l’expression d’un seul gène. Elle peut influencer le comportement de tout un circuit après une épreuve. C’est la raison pour laquelle ces travaux ont attiré autant d’attention. Les auteurs n’ont pas simplement identifié une trace laissée par le stress ; ils ont mis au jour une partie de la réponse protectrice du cerveau lui-même. Bristol a plus tard décrit cette réponse comme un « frein moléculaire » sur les signaux liés à l’anxiété.
Du gène à la structure du neurone : un mécanisme décrypté
L’une des forces de cette étude est sa vision équilibrée : le stress ne produit pas uniquement des changements délétères, il active aussi une réponse qui semble les contrer. L’article de Nature Communications rapporte que le miR-483-5p est régulé à la hausse dans l’amygdale des souris mâles après un stress aigu, s’accumulant dans le compartiment synaptique des neurones. Selon les auteurs, cette molécule peut « contrebalancer les effets néfastes du stress », une formulation qui suggère une modération plutôt qu’une suppression totale. Le cerveau semble recruter un mécanisme de défense intégré pour contenir la réponse au stress.
Le mécanisme est devenu plus clair lorsque les chercheurs ont examiné les gènes supprimés par le miR-483-5p. En croisant plusieurs bases de données, ils ont réduit une large liste de cibles potentielles à 12 gènes pertinents. Les tests expérimentaux ont ensuite affiné l’image : le miR-483-5p réprimait trois gènes associés au stress, à savoir Pgap2, Gpx3 et Macf1. Parmi eux, Pgap2 est apparu comme le candidat le plus important. C’est là que l’étude a dépassé le stade de la simple association. La Dre Valentina Mosienko, l’une des principales auteures, a déclaré que cette voie « offre un potentiel énorme » pour de futures thérapies, car elle a été tracée du stress jusqu’à la modification du comportement, en passant par la répression d’un gène et l’altération de la structure neuronale.
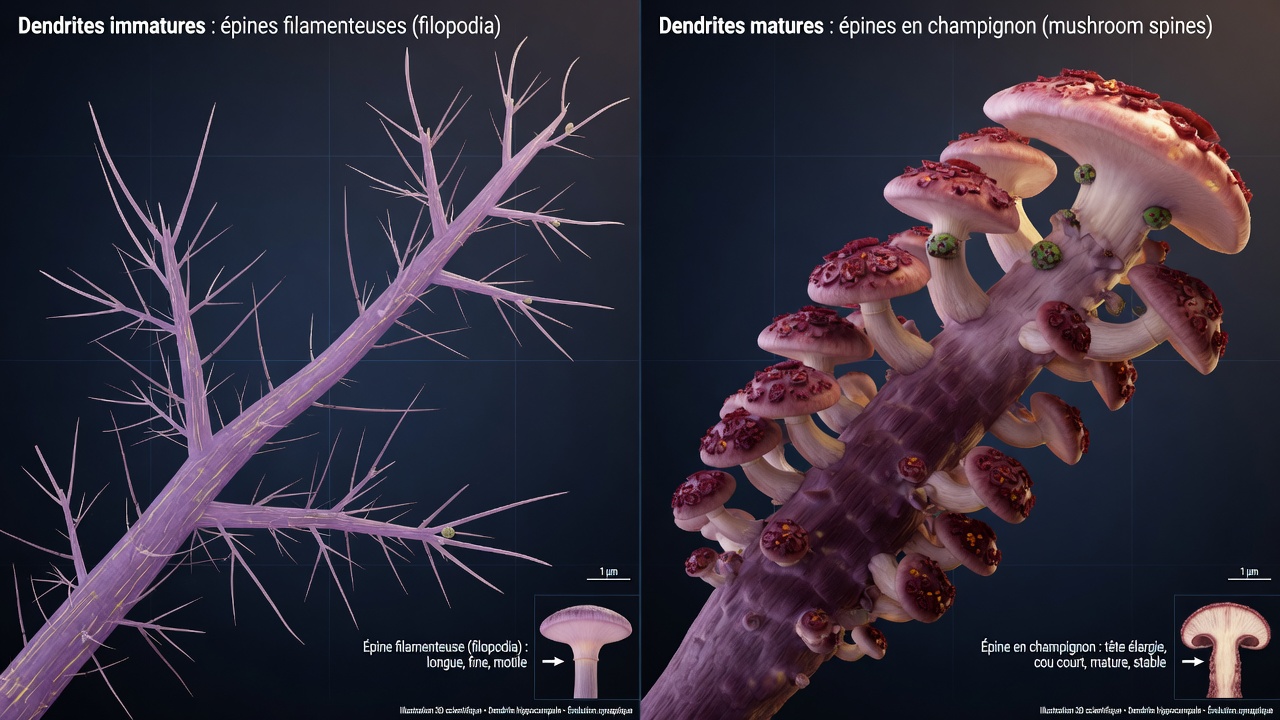
L’étude est devenue la plus convaincante en se concentrant sur le gène Pgap2. Lorsque le miR-483-5p augmentait, les branches dendritiques distales des neurones se contractaient, et les filopodes immatures se transformaient en épines dendritiques matures en forme de champignon. Ces dernières sont associées à des connexions synaptiques plus fortes et plus stables, impliquées dans la formation et le stockage de la mémoire émotionnelle. Les auteurs ont rapporté une augmentation d’environ 60% de ces épines matures. Pour prouver que Pgap2 était bien le moteur de ces effets, ils ont montré que la suppression de ce gène reproduisait les changements, et que la restauration d’une forme de Pgap2 résistante au miR-483-5p les bloquait. Cette expérience dite de sauvetage est une preuve solide du lien de causalité. Dans un contexte où le stress est souvent lié à une prolifération dendritique associée à l’anxiété, ce rétrécissement pourrait représenter une correction protectrice.
Moins d’anxiété chez la souris, mais des conclusions prudentes

L’étude est restée cohérente jusqu’à l’analyse du comportement. Après avoir surexprimé le miR-483-5p dans l’amygdale basolatérale, les chercheurs ont testé les souris dans un labyrinthe en croix surélevé, un test standard pour mesurer les comportements anxieux. Les souris modifiées ont passé environ 40% de temps en plus dans les bras ouverts du labyrinthe par rapport aux témoins, un signe de réduction de l’anxiété. Fait important, le nombre total d’entrées dans les bras n’a pas changé, ce qui écarte un effet de sédation ou une modification générale de l’activité motrice. La suppression du gène Pgap2 a produit des résultats similaires.
À ce stade, l’article avait construit une séquence complète, allant de l’exposition au stress à l’enrichissement synaptique, en passant par la répression d’une cible génétique, le remodelage dendritique et enfin le comportement. C’est ce qui a permis aux auteurs d’écrire que le miR-483-5p était « suffisant pour conférer » un comportement moins anxieux. Dans un domaine de recherche saturé de déclarations générales, cette cohérence est une force majeure qui offre une voie claire pour les travaux futurs.
Malgré ces points forts, une interprétation prudente reste nécessaire. Il s’agit d’une étude sur des souris, et plus précisément des souris mâles, utilisant un modèle de stress aigu de 6 heures et une manipulation virale directe d’une seule région de l’amygdale. Les troubles anxieux humains sont bien plus complexes, influencés par des facteurs environnementaux, génétiques, des traumatismes et le développement. Le communiqué de presse de Bristol gère bien cet équilibre, qualifiant la découverte de « premier tremplin » vers des traitements améliorés. L’étude n’a pas produit un médicament pour l’homme, ni prouvé que toute forme d’anxiété peut être ‘éteinte’. Elle a identifié une voie de l’amygdale qui semble amortir les effets du stress chez l’animal. Pour la médecine de demain, c’est un résultat majeur qui suggère que de nouveaux traitements pourraient un jour renforcer les mécanismes de résilience du cerveau lui-même.
Créé par des humains, assisté par IA.