Un mécanisme géologique millénaire de capture du co₂ réduit à quelques heures en laboratoire
Auteur: Adam David
Quand la géologie rencontre l’urgence climatique

Le temps presse face à la crise climatique. Alors que les objectifs ambitieux de l’Accord de Paris semblent s’éloigner chaque année, la nécessité de développer des technologies de capture du carbone efficaces n’a jamais été aussi cruciale. Dans ce contexte, une équipe de chercheurs israéliens vient peut-être de réaliser une avancée décisive : ils ont réussi à condenser en quelques heures seulement un mécanisme géologique de séquestration du CO₂, qui prendrait naturellement des milliers d’années.
Des efforts insuffisants face à l’augmentation des émissions

La pression sur la recherche scientifique est immense. Malgré l’engagement international de limiter le réchauffement à 1,5 °C pris en 2016, les efforts actuels pour réduire les émissions de gaz à effet de serre restent largement insuffisants. Le dernier rapport du Programme des Nations Unies pour l’Environnement (PNUE) le confirme de manière cinglante : si la tendance se maintient, la hausse moyenne des températures mondiales dépassera, au moins temporairement, le seuil critique de 1,5 °C d’ici le début des années 2030.
Pire encore, les émissions continuent de grimper, défiant toutes les tentatives de stabilisation. Elles ont atteint un niveau astronomique en 2023, s’établissant à 53 milliards de tonnes équivalent CO₂, soit une augmentation de 1,9 % par rapport à l’année précédente. Une grande partie de ce fardeau, près de 40 %, provient d’ailleurs de la production d’électricité, majoritairement (73 %) imputable aux centrales thermiques fonctionnant encore au charbon.
L’altération des carbonates, le modèle naturel

L’approche proposée par les scientifiques de l’Université hébraïque de Jérusalem et de l’Université ouverte israélienne ne sort pas de nulle part. Elle s’inspire directement de l’un des mécanismes les plus puissants de la Terre pour recycler le carbone : l’altération des carbonates. Naturellement, le dioxyde de carbone se dissout dans l’eau de pluie, créant un acide carbonique faible.
Cet acide, au fil du temps, ronge lentement les roches contenant du carbonate de calcium, comme le calcaire et la dolomite, transformant le carbone en ions stables. Ces ions sont ensuite charriés par les rivières jusqu’aux océans, où ils sont séquestrés pour une très longue durée. Le problème, c’est que ce processus est extrêmement lent, et il ne peut suffire, à lui seul, à compenser les volumes gigantesques de CO₂ que nous émettons.
Réduire la géochimie à l’échelle d’un réacteur
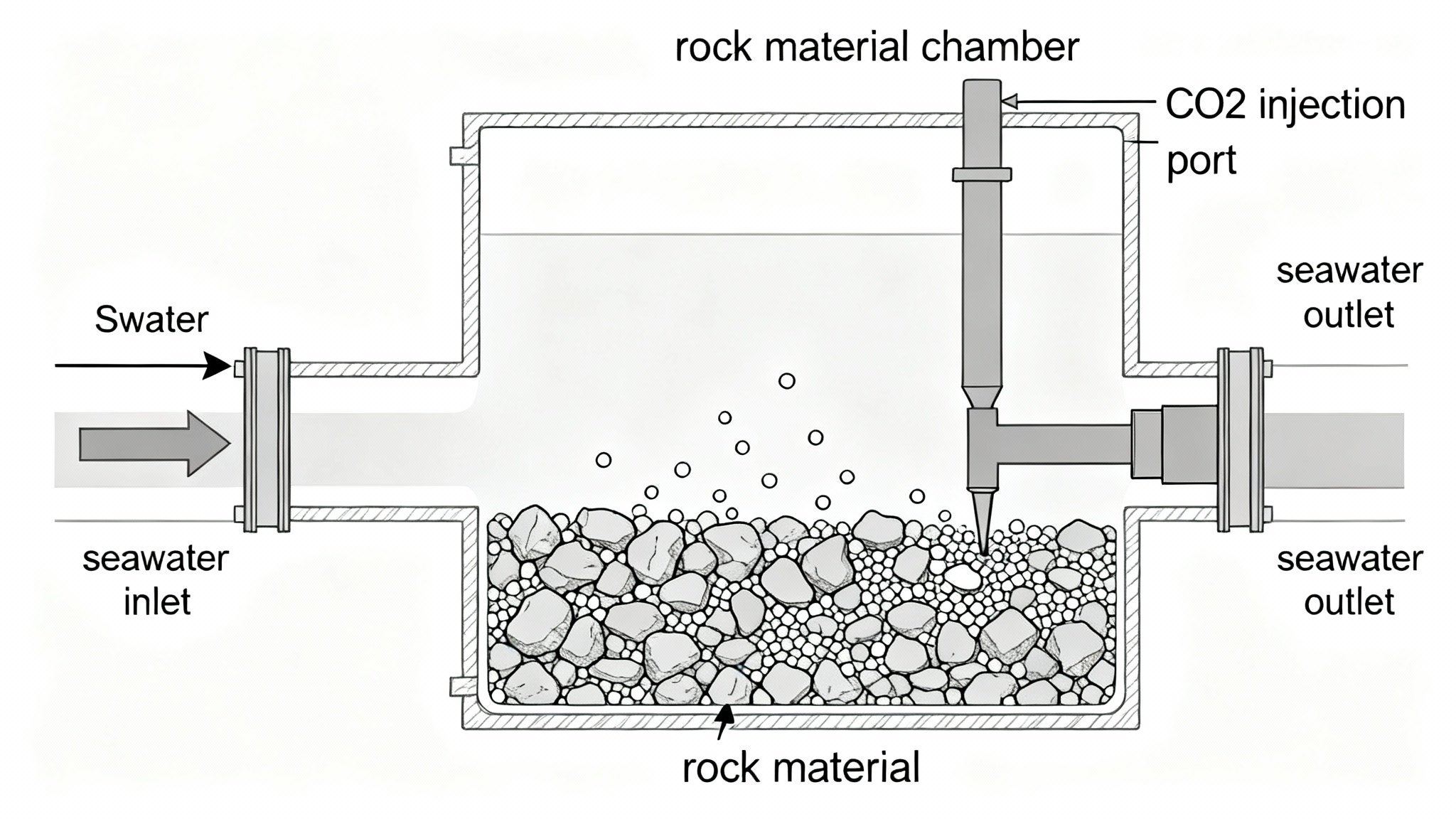
L’équipe de chercheurs, dirigée par Noga Moran, a cherché à reproduire et optimiser cette réaction en circuit fermé. Leur objectif était de transposer « à l’échelle humaine un processus que la Terre pratique depuis des millions d’années », explique Noga Moran au Jerusalem Post. Pour cela, ils ont conçu un réacteur transparent, un véritable laboratoire miniature où ils ont fait circuler de l’eau de mer saturée en CO₂ au contact des roches carbonatées.
L’enjeu consistait à identifier les conditions optimales pour accélérer la dissolution. « Une fois ces conditions définies, nous pouvions transformer un phénomène naturel et lent en un processus contrôlé, mesurable et ajustable », précise Moran dans un communiqué. L’étude, publiée dans la revue Environmental Science & Technology, détaille comment 14 expériences ont permis de cerner les variables clés.
L’importance du débit et de la granulométrie

Les chercheurs ont notamment découvert que le rapport entre le CO₂ et l’eau de mer était essentiel pour l’efficacité du procédé. Un recyclage doux du gaz a par exemple considérablement amélioré les réactions chimiques, tandis qu’un débit trop rapide réduisait le rendement. La granulométrie des roches s’est également révélée fondamentale : les grains plus petits augmentent la surface de contact, favorisant la dissolution du carbone total, mais les grains plus volumineux créent des voies plus fluides qui, paradoxalement, accélèrent la vitesse de réaction globale.
Autre constatation cruciale : la dolomite s’est avérée plus efficace pour la capture et le recyclage du carbone que le calcaire. Elle produit en effet moins de précipités secondaires de carbonate, qui pourraient potentiellement relâcher à nouveau du carbone dans l’atmosphère. Ces ajustements ont permis au système de convertir environ 20 % du CO₂ introduit en carbone inorganique dissous.
Vers une capture industrielle abordable

Ce taux de conversion initial de 20 % peut sembler faible, mais les chercheurs estiment qu’il existe une marge d’amélioration significative via des ajustements techniques. Ces résultats posent en fait les bases des futurs protocoles industriels pour ce procédé d’altération des carbonates amélioré. Les experts soulignent ainsi « la faisabilité de la stimulation de l’altération des carbonates dans un réacteur à système ouvert et offrent des stratégies pratiques pour la séquestration du carbone issu des centrales électriques. »
Le principal atout de cette technologie réside dans son coût potentiel : le système s’appuie sur des matériaux abondants et peu onéreux (eau de mer, calcaire, dolomite). S’il parvient à être mis à l’échelle, il pourrait donc offrir une solution de séquestration du carbone directement applicable aux grandes sources d’émission industrielles, dépassant le seul secteur de la production d’électricité.
Ce contenu a été créé avec l’aide de l’IA.