Un changement de cap radical venu de Barcelone

Depuis des années, la recherche sur la maladie d’Alzheimer semblait suivre une seule et même voie : la lutte acharnée contre les plaques amyloïdes, ces amas de protéines qui s’accumulent dans le cerveau et étouffent progressivement les neurones. Pourtant, une équipe de scientifiques de l’Université de Barcelone vient de remettre en question ce dogme, suggérant que la médecine pourrait s’être acharnée sur le mauvais coupable.
Dans une étude publiée dans la revue Molecular Therapy, ces biologistes présentent une approche totalement nouvelle. Partant du principe que les traitements actuels s’attaquaient aux conséquences de la maladie plutôt qu’à sa racine, ils ont mis au point un composé inédit. Celui-ci est capable de « reprogrammer » directement la machinerie génétique de notre cerveau.
Cette avancée est spectaculaire. Elle ne vise plus seulement à freiner la progression de la démence, un objectif déjà difficile à atteindre, mais ouvre la porte à une potentielle réparation des dégâts. En laboratoire, les premiers résultats montrent déjà une capacité à effacer certaines séquelles de la maladie.
Les limites des traitements actuels : quand les plaques ne sont qu’un symptôme
Jusqu’à présent, l’arsenal thérapeutique contre Alzheimer reposait principalement sur des anticorps monoclonaux, comme le lecanemab ou le donanemab. Ces médicaments, véritables prouesses techniques, sont conçus pour faire le ménage dans le cerveau en ciblant et en détruisant les amas de protéines bêta-amyloïdes et tau.
Malgré des milliards investis dans leur développement, leur efficacité clinique reste limitée. Lorsqu’ils sont administrés à un stade très précoce de la maladie, ils parviennent à ralentir le déclin cognitif d’environ 30 %. C’est une victoire, certes, mais une victoire partielle. Le principal écueil demeure : ces traitements sont incapables de restaurer la mémoire déjà perdue.
Cette incapacité à inverser la tendance a poussé les chercheurs à une remise en question fondamentale. Et si ces fameuses plaques n’étaient finalement que les cicatrices laissées par la maladie, et non son véritable moteur ? Une hypothèse qui change radicalement la perspective de la recherche.
Une nouvelle cible : l’épigénome humain
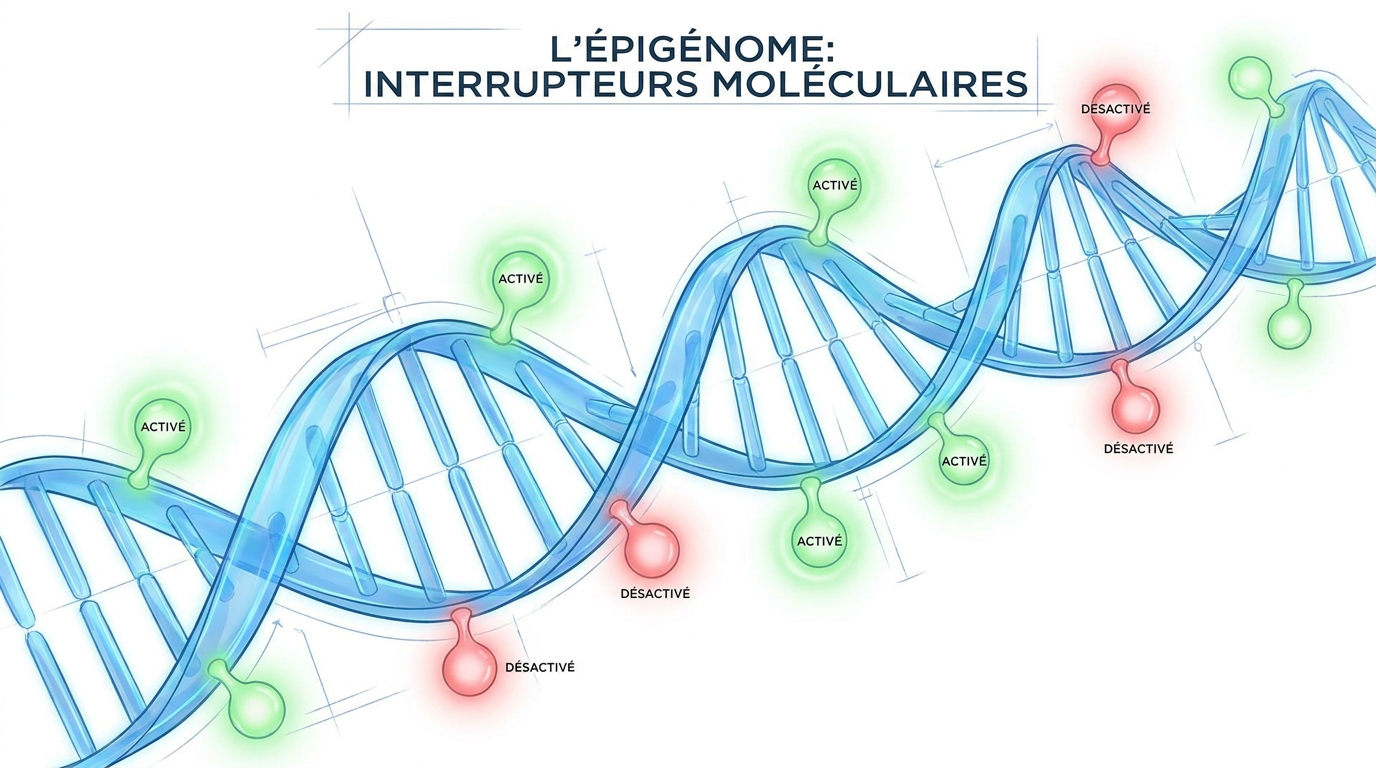
C’est dans ce contexte de remise en question qu’intervient le composé FLAV-27. Cette molécule développée par l’équipe de Barcelone change complètement de champ de bataille. Au lieu de nettoyer les protéines toxiques qui s’accumulent, ce traitement s’attaque directement à l’épigénome humain.
Qu’est-ce que l’épigénome ? Pour simplifier, on peut le voir comme le système d’interrupteurs de notre corps. Il ne modifie pas notre ADN, mais il contrôle quels gènes sont activés ou éteints à un moment donné. C’est lui qui orchestre l’expression de notre patrimoine génétique.
Dans le cas de la maladie d’Alzheimer, les recherches ont montré qu’une enzyme spécifique, baptisée G9a, semble s’emballer. Elle se met à « réduire au silence » des gènes qui sont absolument vitaux pour le bon fonctionnement de nos synapses et le traitement de nos souvenirs. Le problème serait donc un dérèglement de la commande génétique elle-même.
FLAV-27 : des résultats en laboratoire qui dépassent les attentes

Le composé FLAV-27 a été conçu pour agir comme un brouilleur extrêmement précis. Sa mission : bloquer chimiquement l’enzyme G9a défaillante. En étant privée de son carburant, l’enzyme est forcée de lâcher prise. Cette action permet aux gènes essentiels à la mémoire de s’exprimer à nouveau normalement, restaurant ainsi une fonction biologique cruciale.
Les résultats publiés par l’équipe scientifique ont dépassé leurs propres attentes. Lors des premiers tests menés sur des nématodes, de petits vers utilisés en laboratoire, le FLAV-27 a non seulement prolongé leur durée de vie, mais il a aussi amélioré la respiration de leurs cellules et leur mobilité.
Le succès s’est confirmé sur des modèles plus complexes : des souris atteintes de formes précoces et tardives d’Alzheimer. En calmant le dérèglement génétique, le composé a réalisé un exploit inédit. Il a restauré les performances de la mémoire spatiale, relancé les comportements sociaux des rongeurs et même réparé des connexions synaptiques endommagées. Mieux encore, cette reprogrammation a entraîné une diminution naturelle des plaques amyloïdes, confirmant qu’elles sont bien un symptôme secondaire d’un chaos génétique plus profond.
De l’espoir, mais un long chemin à parcourir

Ce renversement de la maladie en laboratoire constitue une lueur d’espoir immense pour des millions de familles touchées par Alzheimer. Cependant, la prudence reste de mise. Le FLAV-27 doit encore franchir la redoutable et longue étape des essais cliniques sur l’Homme pour prouver son efficacité et son innocuité.
Avant qu’un tel médicament puisse un jour être prescrit, l’équipe de recherche va devoir mener des études toxicologiques approfondies. La réglementation exige que ces tests soient réalisés sur au moins deux espèces animales distinctes afin de s’assurer que cette reprogrammation épigénétique est sans danger sur le long terme.
Quoi qu’il en soit, cette avancée est porteuse d’un message fort. Elle prouve que la démence n’est peut-être pas une fatalité irréversible. Elle pourrait plutôt être considérée comme une sorte d’erreur de codage, une erreur que la science est peut-être enfin en train d’apprendre à corriger.
Selon la source : demotivateur.fr